14
6月
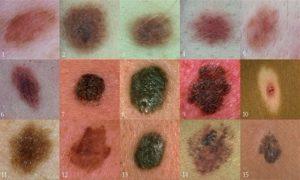
黑色素瘤的病因与危险因素
黑色素瘤(Melanoma)是一种常见的皮肤癌,它通常起源于皮肤表面的黑素瘤或良性痣。尽管黑色素瘤的发病率相对较低,但它的致命性却较高,尤其是在晚期诊断时。黑色素瘤的发展与许多病因和危险因素密切相关,了解这些因素对于预防和及早诊断黑色素瘤至关重要。 1. 遗传因素 黑色素瘤的发病与个体的遗传因素密切相关。研究表明,具有家族史的人患黑色素瘤的风险较高。如果家族中有黑色素瘤患者,那么其他家庭成员患病的可能性也会增加。此外,一些特定的基因突变,如CDKN2A和CDK4基因的突变,与黑色素瘤的发生有关。 2. 长期日晒暴露 长期暴露在紫外线下是导致黑色素瘤的主要危险因素之一。过度日晒或在强烈阳光下工作... 查看详情
14
6月
舒立瑞(依库珠单抗)在中国获批改善难治性全身型重症肌无力
2023年6月13日,阿斯利康公司宣布在中国获得了依库珠单抗注射液eculizumab(商品名称Soliris,舒立瑞)的新适应症批准,这是一项重要的里程碑。依库珠单抗是中国首个也是唯一一个获批用于治疗抗乙酰胆碱受体(AChR)抗体阳性的难治性全身型重症肌无力(gMG)成人患者的补体抑制剂。这一消息为那些曾因未能找到有效治疗方法而备受困扰的患者和医疗界带来了希望。 研究结果证实依库珠单抗的疗效和安全性 阿斯利康公司的公告指出,依库珠单抗获得中国国家药品监督管理局(NMPA)的批准,主要是基于一项关键的III期临床试验(REGAIN研究)结果,该研究证实了该药对难治性gMG成人患者的疗效和安全性... 查看详情
14
6月
FDA加速批准Zynyz用于治疗转移性或复发性局部晚期梅克尔细胞癌
罕见而致命的皮肤癌梅克尔细胞癌(MCC)是一种令人担忧的疾病。然而,美国食品和药物管理局(FDA)已加速批准Zynyz(retifanlimab-dlwr)用于治疗成年人的转移性或复发性局部晚期MCC。这一批准有望为患者带来新的治疗选择,并为改善其生存和生活质量带来曙光。 梅克尔细胞癌:一种罕见而致命的皮肤癌 梅克尔细胞癌是一种罕见的皮肤癌,起源于表皮中的梅克尔细胞。这些细胞位于接收触觉的神经末梢附近,并含有可能充当激素的物质。因此,MCC有时也被称为皮肤神经内分泌癌。 MCC通常发生在头部和颈部区域,但也可能在其他暴露在阳光下的皮肤区域,如手臂和腿部。它表现为单个、无痛的红紫色皮肤结节,并且... 查看详情
14
6月
Zynyz为默克尔细胞癌MCC患者带来突破性免疫治疗选择
新疗法的引入有望改变MCC患者的治疗前景,为他们提供更多的治疗选择和延长生存期的机会。然而,尽管免疫疗法带来了希望,但仍然需要进一步的研究和临床实践来深入了解其长期疗效和安全性。 免疫治疗:开启MCC治疗新纪元 默克尔细胞癌(MCC)作为一种恶性程度较高的皮肤癌,一直以来都是一个治疗难题。它具有快速进展和差劲的预后,使得患者面临着巨大的生存压力。然而,近年来,免疫治疗的突破为MCC患者带来了新的曙光。 免疫疗法的突破 免疫疗法已经成为多种恶性肿瘤治疗的重要手段,而MCC也不例外。目前,已有多款PD-1/PD-L1抑制剂获得了治疗MCC的批准,并在临床实践中展现出良好的疗效。 新的PD-1单抗Z... 查看详情
13
6月
PREVYMIS® (Letermovir)获批用于预防高风险成人肾移植受者的CMV疾病
美国食品和药物管理局(FDA)已经批准PREVYMIS®(Letermovir)莱特莫韦用于成人肾移植受者的新适应症。这一适应症旨在预防高风险成人肾移植受者(供体CMV血清阳性/受体CMV血清阴性[D+/R-])患上巨细胞病毒(CMV)疾病。 PREVYMIS联合阿昔洛韦用于肾移植受者的CMV预防:P002试验结果 该适应症的批准是基于一项名为P002的3期、随机、多中心、双盲、活性比较器对照的非劣效性试验(NCT03443869)。该试验共有589名成人肾移植受者(CMV D+/R-)参与,他们被随机分为两组,一组接受PREVYMIS联合阿昔洛韦(n=292),另一组接受缬更昔洛韦联合阿昔洛... 查看详情
13
6月
XEOMIN获英国批准,助力下肢痉挛患者迈向康复之路
2023年6月7日,Merz Therapeutics荣获英国药品和保健产品监管机构(MHRA)的批准,将其产品XEOMIN®的治疗范围扩展至治疗影响踝关节的下肢局灶性痉挛。这一批准为英国的痉挛患者提供了更全面的支持,使他们能够获得更有效的治疗。 扩大适应症范围以提供全面支持 Merz Therapeutics荣获英国MHRA的批准,将XEOMIN®用于治疗下肢局灶性痉挛,这是该药物之前仅用于治疗上肢痉挛的批准的进一步扩展。这一扩大的适应症范围为英国需要综合治疗的痉挛患者提供了更全面的支持和选择。 新的治疗方案和剂量 根据新的治疗适应症,XEOMIN®在治疗下肢痉挛时的最大剂量为每次注射400... 查看详情
13
6月
儿童功能性便秘新药LINZESS® (linaclotide)获FDA批准
美国食品和药物管理局(FDA)已批准LINZESS® (linaclotide)利那洛肽作为一种日常治疗,用于治疗6至17岁的功能性便秘儿童患者。这是FDA首次批准针对该患者人群功能性便秘的处方疗法。 为功能性便秘儿童患者提供新的治疗选择 功能性便秘是一种慢性疾病,儿童患者表现为排便困难、排便次数减少以及排便时的困难或疼痛。据估计,在美国有600万6至17岁的儿童受到这种疾病的影响。然而,以往对于这一患者人群的治疗选择相对有限。 基于关键研究的临床效果验证 FDA的批准是基于一项大型、多中心、双盲、III期研究的结果。该研究对328名6至17岁的功能性便秘患者进行了评估,这些患者被随机分配接受... 查看详情
13
6月
基因疗法药物Upstaza治疗严重AADC缺乏症
基因疗法药物Upstaza(eladocagene exuparvovec)是一项创新的治疗方法,针对严重的芳香族L-氨基酸脱羧酶(AADC)缺乏症而开发。AADC缺乏症是一种罕见的遗传性疾病,影响神经系统功能,导致患者在发育、肌肉张力和运动控制方面出现问题。通过引入AADC基因的功能版本,Upstaza有望改善患者的症状,为他们带来重要的健康改善。本文将介绍Upstaza的使用方法、作用机制、临床研究结果以及安全性和监管措施。 Upstaza的使用方法 在经验丰富的脑部手术医生的监护下,Upstaza只能通过处方购买,并在手术室内进行注射治疗。该药物通过脑内输注的方式给予患者,然后进行脑部扫... 查看详情
13
6月
Upstaza疗法为AADC缺陷患者带来新的希望与治疗选择
在医学领域,科技的突破常常带来新的希望和机遇。一项重大的科技创新取得了突破性进展,首个治疗罕见遗传性神经系统疾病AADC缺陷的疗法Upstaza(eladocagene exuparvovec)为AADC患者带来新的治疗选择,为罕见遗传性神经系统疾病的治疗开辟新的道路。 AADC缺陷的严重性及其治疗需求 AADC缺陷是一种极为罕见的遗传性疾病,通常在婴儿出生后的第一年内出现症状。该疾病是由于产生AADC酶所需基因发生变化,该酶在大脑和神经系统的正常功能中起着重要作用。这导致AADC患者发育迟缓、肌肉张力弱和无法控制肢体运动,严重影响他们的生活质量。目前,针对AADC缺陷的治疗选择非常有限,患者... 查看详情
13
6月
科技创新突破!Upstaza成为首个治疗AADC缺陷的疾病修复基因疗法
基因疗法在医学领域中正逐渐展现出巨大的潜力。PTC Therapeutics公司的Upstaza™(eladocagene exuparvovec)获得了欧洲委员会的营销授权,成为首个用于治疗芳香族L-氨基酸脱羧酶(AADC)缺陷的疾病修复治疗。该治疗不仅是首个直接注入脑部的市场上销售的基因疗法,更为患者和基因疗法领域带来了希望。 重要里程碑的达成 PTC Therapeutics首席执行官Stuart W. Peltz博士表示,欧洲委员会对Upstaza用于治疗AADC缺陷的批准是对患者、PTC以及整个基因疗法领域的重要里程碑。作为唯一获得批准用于AADC缺陷患者的疾病修复治疗,PTC Th... 查看详情