11
12月
替尔泊肽Mounjaro在体重减轻方面比竞争对手的减肥药表现更为出色
随着全球肥胖问题的不断加剧,寻找更有效的体重管理药物变得尤为重要。最新的研究通过对Eli Lilly的Mounjaro(Tirzepatide,替尔泊肽/替西帕肽)和Novo Nordisk的肥胖药物进行比较,发现Mounjaro在体重减轻方面表现更为出色。 Mounjaro相较Novo Nordisk药物更为有效 根据对健康记录和其他数据的分析,超重或肥胖成年人使用Eli Lilly的Mounjaro比使用Novo Nordisk的肥胖药物效果更佳。在治疗开始的一年内,接受tirzepatide治疗的患者(Mounjaro和Zepbound的活性成分)中,有42.3%的人体重减轻至少15%,... 查看详情
11
12月
Navitoclax联合鲁索利替尼在骨髓纤维化患者中显著减少脾脏体积
最新的临床研究显示,Navitoclax与鲁索利替尼(Ruxolitinib,Jakafi)联合使用,对患有骨髓纤维化的患者产生了显著影响。这项在第三期TRANSFORM-1研究中取得的结果表明,与鲁索利替尼加安慰剂相比,Navitoclax与鲁索利替尼联合治疗在24周时显著减少了35%或更多的脾脏体积(SVR35W24)。然而,在两组之间的总症状评分(TSS)4.0上并未观察到显著差异。 研究方法 TRANSFORM-1研究(NCT04472598)包括125名接受联合治疗的患者和127名接受对照治疗的患者。联合治疗组中,患者平均年龄为70岁,时间从诊断到入组为8个月,以原发性骨髓纤维化患者... 查看详情
11
12月
Odronextamab在复发/难治性弥漫大B细胞淋巴瘤患者中持续显示出安全、有效
随着对复发/难治性弥漫大B细胞淋巴瘤(R/R DLBCL)患者的最终分析的公布,Odronextamab(REGN1979)单药治疗在疗效方面表现出令人鼓舞的结果,同时在安全性方面保持可控制的良好表现。ELM-2试验的最终分析结果在2023年美国血液学年会上被呈现,显示Odronextamab治疗在复发/难治性弥漫大B细胞淋巴瘤患者中,取得了52%的客观缓解率(ORR),在完全缓解患者中展现出振奋人心的无进展生存(PFS)和总生存(OS)。 Odronextamab的疗效数据 亚特兰大希望之城癌症治疗中心的血液恶性肿瘤医学主任,Sabarish Ram Ayyappan博士,在会议上展示了这项... 查看详情
11
12月
光疗法有助于改善阿尔茨海默病患者的心理行为症状
2023年12月8日报道,光疗法在阿尔茨海默病患者中与显著改善睡眠和心理行为症状相关。一项于12月6日在线发表在《PLOS ONE》期刊的综述表明,光疗法可能成为一种有前途的阿尔茨海默病治疗方式。 光疗法的潜在益处 来自潍坊医学院的Lili Zang及其同事进行了一项系统文献综述,旨在评估光疗法对阿尔茨海默病患者睡眠障碍和心理行为症状的疗效。通过纳入15项随机对照试验(涵盖598名阿尔茨海默病患者),研究人员发现光疗法显著改善了睡眠效果(平均差异[MD]为-2.42),增加了昼夜稳定性(MD为-0.04),减少了昼夜波动性(MD为-0.07)。此外,光疗法还在缓解抑郁(MD为-2.55)以及减... 查看详情
11
12月
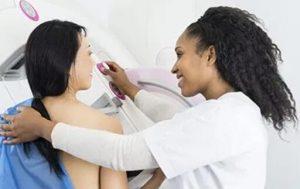
乳腺癌幸存者x光检查次数较少的结果不会更糟
2023年12月8日,来自英国华威大学的研究人员在圣安东尼奥举行的年度圣安东尼奥乳腺癌研讨会上宣布了一项关于乳腺癌幸存者检查频率的研究结果。该研究发现,对于50岁及以上的女性,距离诊断三年后,相较于每年一次的乳腺X光检查,减少检查频率并不会导致不良结果。 研究设计与对象 研究由Janet A. Dunn博士领导,采用了多中心、随机、对照的三期试验,比较了每年一次与每两年一次(保留手术者)以及每三年一次(乳腺切除者)乳腺X光检查的效果。研究纳入了5,235名乳腺癌女性患者,她们在2014年4月至2018年9月间被随机分配,其中87%的患者患有浸润性疾病。 研究结果 在随访中位数为5.4年的时间内... 查看详情
11
12月
FDA批准Cresemba(艾沙康唑)治疗1岁及以上儿童的侵袭性曲霉病和毛霉菌病
在医学领域,罕见病的治疗一直是科研和制药领域关注的焦点之一。2023年12月8日,Astellas Pharma US, Inc.(安斯泰来)宣布,美国食品和药物管理局(FDA)已批准Cresemba®(isavuconazole,艾沙康唑)用于治疗1岁及以上儿童的侵袭性曲霉病(IA)和侵袭性毛霉菌病(IM)。这一批准标志着在儿科领域获得有效抗真菌疗法的重要突破,将为免疫功能低下的年幼患者提供更多治疗选择。 儿科患者的新希望 Cresemba成为目前唯一被批准用于治疗1岁及以上儿童IA和IM的唑类抗真菌疗法。这一突破性的批准是基于两项儿科临床研究的结果,为在这一特殊人群中提供安全有效的治疗方案... 查看详情
10
12月
FDA批准Lyfgenia治疗12岁及以上患有血管闭塞危象的镰状细胞贫血病
在罕见病治疗领域,基因疗法的发展为一些严重疾病的患者带来了新的希望。2023年12月8日,美国FDA宣布批准bluebird bio公司研发的基因疗法Lyfgenia用于治疗12岁及以上患有镰状细胞贫血病(SCD)且有血管闭塞事件(VOE)史的患者。这一新治疗的获批标志着罕见病领域的又一次科技突破,为患者提供了新的生存和生活质量的机会。 临床数据分析 Lyfgenia的批准基于对12至50岁患有SCD和VOE病史的患者进行的一项为期24个月的多中心研究的数据分析。通过对患者在接受Lyfgenia输注后6至18个月内达成VOE完全消退(VOE-CR)的评估,研究显示在32例患者中有28名(88%... 查看详情
10
12月
欧盟批准Elrexfio(Elranatamab)治疗复发或难治性多发性骨髓瘤
在罕见病治疗领域,医学科技的不断创新为患者带来了新的曙光。2023年12月8日,辉瑞公司宣布其研发的CD3/BCMA双抗ELREXFIO(elranatamab)获得欧盟委员会(EC)批准,用于治疗复发或难治性多发性骨髓瘤(R/R MM)。这一治疗的成功批准标志着多发性骨髓瘤领域迈向了新的里程碑。 临床试验的积极成果 ELREXFIO的获批是基于MagnetisMM-3研究队列A的积极数据。这项研究旨在评估elranatamab单药治疗R/R MM的安全性和有效性。在接受elranatamab治疗前曾接受过多次治疗的患者中,总缓解率(ORR)为58%,而维持至少9个月缓解的患者比例高达82%。... 查看详情
09
12月
FDA批准CASGEVY治疗12岁及以上患有复发性血管闭塞危象的镰状细胞贫血病
在医学科技的快速发展下,基因编辑疗法为一系列罕见病提供了新的治疗前景。2023年12月08日,美国FDA宣布批准Vertex Pharmaceuticals和CRISPR Therapeutics联合研发的CRISPR/Cas9基因编辑疗法Casgevy(exagamglogene autotemcel,exa-cel)上市,用于治疗12岁及以上患有复发性血管闭塞危象的镰状细胞贫血病(SCD)患者。这一里程碑性的决定为SCD患者带来了新的曙光。 Casgevy:CRISPR基因编辑疗法的新突破 Casgevy是首款获得FDA批准的CRISPR基因编辑疗法,标志着基因编辑技术在医学治疗领域的进一... 查看详情
09
12月
PIVLAZ(克拉佐生坦钠)在韩国获批:预防脑血管痉挛和aSAH手术后脑缺血症状
随着医学科技的飞速发展,新的药物不断涌现,为患者提供了更多治疗选择。近日,Sosei公司宣布其旗下产品PIVLAZ™(clazosentan sodium,克拉佐生坦钠)已经在韩国获得批准,用于预防脑血管痉挛相关的脑梗死以及动脉瘤性蛛网膜下腔出血(aSAH)术后脑缺血症状。 全新选择:PIVLAZ™的草创性治疗 PIVLAZ™是一种克拉佐生坦钠,属于选择性内皮素A(ETA)受体拮抗剂。这一创新性治疗方案在预防脑血管痉挛、血管痉挛相关的脑梗死,以及动脉瘤性蛛网膜下腔出血(aSAH)术后的脑缺血症状方面显示出巨大潜力。 临床数据支持:科学与实践的完美结合 PIVLAZ™的MFDS批准建立在Sose... 查看详情