VILTEPSO VILTOLARSEN
【商品名称】:VILTEPSO
【通用名称】:VILTOLARSEN
Viltepso(viltolarsen)说明书
【Viltepso(viltolarsen)适应症】
Viltepso(viltolarsen)为反义疗法药物,适用于经确认存在肌营养不良蛋白基因缺陷、且适合53号外显子跳跃治疗的杜氏肌营养不良症(DMD)患者。
【Viltepso(viltolarsen)生产企业】
NS Pharma
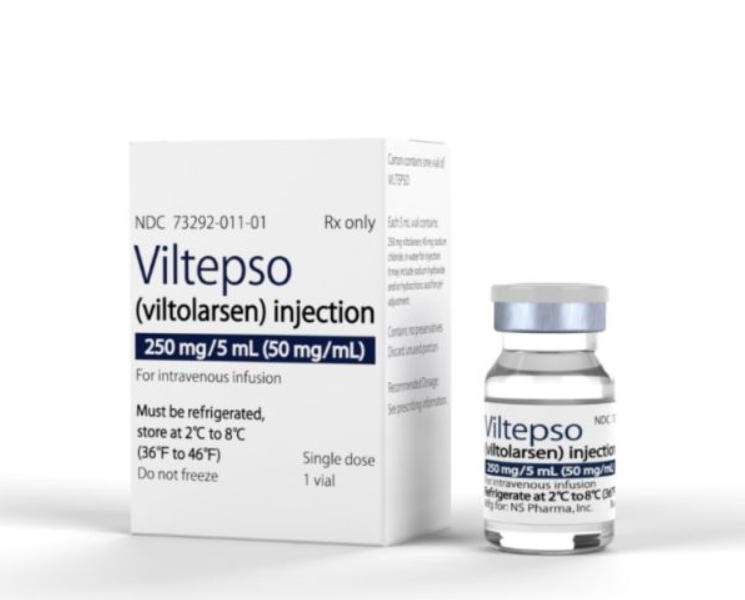
【Viltepso(viltolarsen)规格】
本品为单剂量瓶装,每瓶含viltolarsen 250毫克/5毫升。
【Viltepso(viltolarsen)作用机制】
杜氏肌营养不良症(DMD)是一种常见的致命性进行性肌肉萎缩疾病,主要发生于男性儿童。DMD患者体内的肌营养不良蛋白功能异常,该蛋白对肌肉健康至关重要,其功能异常会导致肌肉无力和肌肉量减少。
这种异常产生源于DMD基因的突变。大多数基因由交替排列的“外显子”和“内含子”组成,外显子包含蛋白质合成的遗传密码,内含子则无编码功能。细胞需先复制基因形成信使RNA(mRNA),再对mRNA进行“剪接”——切除内含子区域并连接外显子,最终形成完整的蛋白质编码序列。
部分DMD病例中,DMD基因的特定片段缺失会导致外显子无法正常拼接,破坏编码序列,进而产生无功能的肌营养不良蛋白。
Viltepso属于反义寡核苷酸,含有人工mRNA片段,可通过重新拼接外显子纠正编码序列异常。本品专为DMD基因的53号外显子设计,仅对适合53号外显子跳跃治疗的突变型患者有效。
【Viltepso(viltolarsen)获批情况】
Viltepso(viltolarsen)已获以下机构批准用于适合53号外显子跳跃治疗的杜氏肌营养不良症(DMD)患者:
美国食品药品监督管理局(FDA),批准日期为2020年8月12日;日本药品和医疗器械局(PMDA),批准日期为2020年3月25日。
FDA为Viltepso授予加速批准资格,并给予优先审评、快速通道、孤儿药及罕见儿科疾病认定;PMDA为其授予“先驱指定”(即日本版突破性疗法认定)、孤儿病认定及条件性早期批准制度认定。
本品可能已在上述提及之外的地区获批,若需了解特定国家的获批情况,可联系支持团队咨询。
【Viltepso(viltolarsen)用法用量】
标准剂量为每周一次静脉输注Viltepso 80毫克/千克,输注时间不少于1小时。
开始Viltepso治疗前,应检测血清胱抑素C、尿试纸及尿蛋白肌酐比值,治疗期间建议定期监测肾功能。
关于本品的完整用法用量信息,可查阅参考资料中的处方信息。需结合个体情况制定给药方案并评估药物相互作用,具体请遵循诊疗建议。
【Viltepso(viltolarsen)不良反应】
常见不良反应
处方信息中记载的常见(发生率≥15%)不良反应包括:上呼吸道感染、注射部位反应、咳嗽、食欲减退(发热)。
严重不良反应
处方信息中未提及本品相关严重不良反应。
完整的不良反应列表请参考官方处方信息。
【Viltepso(viltolarsen)临床试验】
美国FDA对Viltepso(viltolarsen)用于适合53号外显子跳跃治疗的杜氏肌营养不良症(DMD)患者的批准,基于1项研究(研究编号NCT02740972)的数据。
该研究为多中心、两阶段、随机Ⅱ期临床试验,旨在评估Viltepso的安全性和有效性,纳入16名4-10岁经确认存在适合53号外显子跳跃治疗突变的男性DMD患儿,患者随机接受高剂量(80毫克/千克)Viltepso、低剂量(40毫克/千克)Viltepso或安慰剂静脉输注。
试验结果
研究主要结局指标包括骨骼肌中肌营养不良蛋白的产生量、身体功能、定量肌肉力量及不良反应。接受Viltepso治疗的患者肌营养不良蛋白产生量增加,输注20-24周后,患者肌肉中肌营养不良蛋白产生得到恢复。
患者报告的不良反应多为轻度至中度,包括咳嗽和上呼吸道感染,无导致治疗中断的不良事件发生。本品安全性和有效性的完整信息,可参考以下产品特性摘要及资源部分内容。
【Viltepso(viltolarsen)适用人群】
Viltepso专门适用于经确认存在遗传突变、且适合53号外显子跳跃治疗的杜氏肌营养不良症(DMD)患者。需通过基因检测确定是否符合治疗条件,并非所有DMD患者均适用本品。
【Viltepso(viltolarsen)治疗局限性】
Viltepso无法治愈杜氏肌营养不良症,其作用机制为通过增加截短型功能性肌营养不良蛋白的产生延缓疾病进展,可能延长肌肉功能保留时间。
【Viltepso(viltolarsen)居家给药注意事项】
Viltepso通常需在医疗环境中进行静脉输注,若考虑居家输注,必须由经过培训的医疗专业人员操作,并监测是否出现即时反应,同时需严格遵循储存和操作说明。
【Viltepso(viltolarsen)药物相互作用】
目前尚无明确的Viltepso药物相互作用记录,但患者需向医疗服务提供者告知所有使用的药物(包括非处方药和补充剂),以确保治疗安全性并便于监测。
【Viltepso(viltolarsen)治疗期间肾功能监测】
治疗前及治疗期间需通过定期评估尿蛋白、尿试纸及血清胱抑素C监测肾功能,若出现异常,可能需进一步检查或调整治疗方案。
【Viltepso(viltolarsen)漏服处理】
若错过预定给药时间,应尽快联系医疗服务提供者获取指导,切勿通过加倍剂量弥补漏输剂量。
【Viltepso(viltolarsen)联合用药】
Viltepso可与皮质类固醇及其他杜氏肌营养不良症标准治疗药物联合使用,但任何联合治疗均需由神经肌肉专科医生监督,以监测是否出现叠加不良反应或药物相互作用。
【Viltepso(viltolarsen)过敏反应体征】
本品过敏反应体征包括输注期间或输注后出现皮疹、瘙痒、肿胀、呼吸困难或胸闷,出现任何上述症状需立即寻求医疗帮助。
【Viltepso(viltolarsen)治疗疗程】
Viltepso为长期治疗药物,需每周给药一次,疗程取决于患者治疗获益情况及是否出现不可接受的不良反应,具体由诊疗医生根据患者个体反应确定。
【温馨提示】
如需要更多Viltepso(viltolarsen)资讯,欢迎与致泰药业联络查询。香港致泰药业是经香港政府卫生署注册的药品批发商,专注于全球新特药品进出口业务。

注:以上资讯来源于网络,并由致泰药业整理编辑(如有错漏,请帮忙指正),只为提供全球最新上市药品的资讯,帮助全球各地华人患者了解国际新药动态,仅供医护人员内部讨论,不作任何用药建议及依据, 如想要进一步了解药品,请咨询主治医师。