GOMEKLI MIRDAMETINIB
【商品名称】:GOMEKLI
【通用名称】:MIRDAMETINIB
GOMEKLI(mirdametinib)说明书
【GOMEKLI生产厂家】
Gomekli Biopharma 制药公司
【GOMEKLI适应症】
Gomekli适用于治疗1型神经纤维瘤病(NF1)患者,针对2岁及以上、存在症状性丛状神经纤维瘤(PN)且无法完全切除的患者提供治疗。
【GOMEKLI规格】
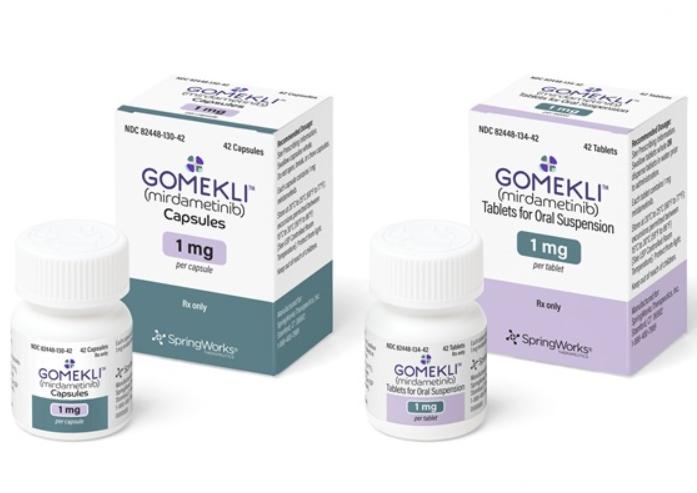
胶囊剂型:
- 1mg(瓶装42粒)
- 2mg(瓶装42粒或84粒)
口服混悬液片剂:
- 1mg(瓶装42片或84片)
【GOMEKLI药物性状】
胶囊:
- 1mg:淡绿色主体,搭配深绿色瓶盖,瓶盖上印有白色标识“MIR 1 mg”。
- 2mg:白色主体,蓝绿色瓶盖,瓶盖上印有白色标识“MIR 2 mg”。
口服混悬液片剂:
- 1mg:白色至淡灰色,椭圆形,带葡萄香味,一侧压印有“S”标识。
【GOMEKLI用法用量】
使用前评估:
- 服用前需进行全面的眼科检查,并通过超声心动图测量射血分数(EF),确保患者适合用药(详细信息见【注意事项】)。
剂型说明:
- 胶囊剂:需整粒吞服,切勿咀嚼、掰开或研碎。
- 口服混悬液片剂:可整片吞服,或溶解于水中后服用(详见【用药指南】)。
推荐剂量:
- 2mg/m²,每日两次(间隔约12小时)。
- 在每个28天治疗周期的前21天服用,可随餐或空腹服用。
- 最大剂量:4mg,每日两次。
- 持续治疗,直至病情恶化或患者无法耐受。
【GOMEKLI禁忌症】
目前未发现绝对禁忌症。
【GOMEKLI警告与注意事项】
眼部毒性:可能引发视网膜静脉阻塞(RVO)、视网膜色素上皮脱离(RPED)及视力模糊。使用前及治疗期间需定期进行眼科检查。如出现视力下降,应根据情况调整剂量或停药。
心脏功能异常:可能影响左心室功能。尚未在LVEF低于55%的患者中进行研究。建议服药前进行心脏超声检查,并在治疗初期每3个月检查一次。
皮肤反应:可能导致皮疹及其他皮肤病症。如有不适,建议使用支持性治疗,严重者需调整剂量或停药。
胎儿风险:本品可能对胎儿造成影响,孕妇禁用。育龄女性服用本品期间及停药后6周内需采取有效避孕措施,男性患者则需在停药后3个月内避免生育。
【GOMEKLI特殊人群用药】
- 哺乳期女性:由于可能影响婴儿健康,服药期间及停药后1周内应避免哺乳。
- 生育能力:可能影响女性生育功能。
- 儿童用药:2岁以下患者的安全性和有效性尚未确立。
- 老年患者:65岁以上患者的药效与年轻人群的差异尚不明确。
- 肾功能损害:轻度至中度肾功能损害(肌酐清除率30-89mL/min)患者无需调整剂量,重度肾功能损害(<30mL/min)患者的用药影响尚未研究。
- 肝功能损害:轻度肝功能损害(胆红素≤ULN且AST>ULN,或胆红素1-1.5倍ULN)患者无需调整剂量,中重度肝功能损害患者的药代动力学尚未研究。
【GOMEKLI不良反应】
- 成人常见不良反应(>25%):皮疹、腹泻、恶心、肌肉关节疼痛、呕吐、疲劳等。
- 儿童常见不良反应(>25%):皮疹、腹泻、肌肉关节疼痛、腹痛、呕吐、头痛、甲沟炎、左心室功能受损、恶心等。
- 严重实验室异常(>2%):
- 成人:肌酸磷酸激酶(CPK)升高。
- 儿童:中性粒细胞减少、肌酸磷酸激酶(CPK)升高。
【GOMEKLI储存方式】
请存放于避光、室温环境(20°C至25°C,即68°F至77°F)。短期存放可在15°C至30°C(59°F至86°F)范围内。
【温馨提示】
如需要更多GOMEKLI(mirdametinib)资讯,欢迎与致泰药业联络查询。香港致泰药业是经香港政府卫生署注册的药品批发商,专注于全球新特药品进出口业务。

注:以上资讯来源于网络,并由致泰药业整理编辑(如有错漏,请帮忙指正),只为提供全球最新上市药品的资讯,帮助全球各地华人患者了解国际新药动态,仅供医护人员内部讨论,不作任何用药建议及依据, 如想要进一步了解药品,请咨询主治医师。