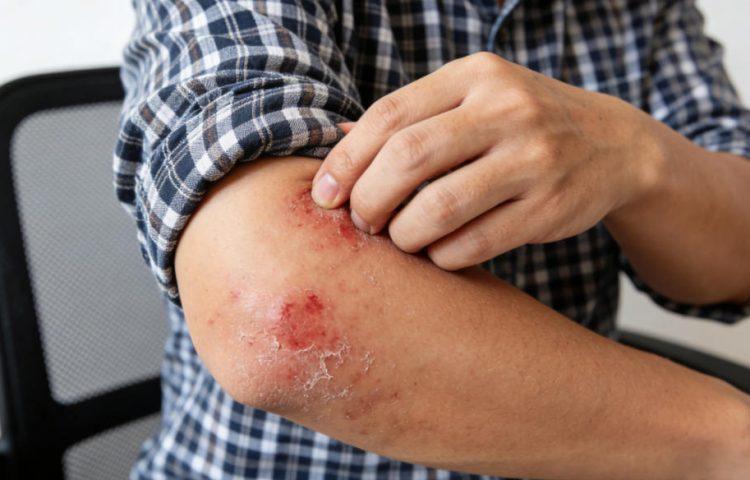
美国FDA批准Adquey(地法米司特1%)用于轻中度特应性皮炎治疗
2026年2月13日,Acrotech Biopharma Inc.宣布,美国食品药品监督管理局已批准非类固醇类药物Adquey(difamilast 1%,地法米司特1%)软膏的新药申请,用于局部治疗2岁及以上成人和儿童患者的轻中度特应性皮炎。
Adquey是一种新型非甾体类局部用磷酸二酯酶4(PDE4)抑制剂,对所有磷酸二酯酶4亚型均显示出抑制活性。其作用机制为通过抑制PDE4的活性,导致细胞内环磷酸腺苷积累,减少多种细胞因子和趋化因子的产生,改变细胞信号传导并降低皮肤中的炎症信号,从而缓解特应性皮炎相关症状,但其发挥治疗作用的具体机制尚不完全明确。
Adquey为局部用软膏剂型,仅供皮肤使用,不可放入眼睛、口腔或阴道内。其推荐使用方式为每天两次,在患处涂抹薄薄一层并完全揉进皮肤,同时避开看起来受感染的皮肤区域。
美国食品药品监督管理局的批准基于多项临床试验,包括关键的Ⅲ期对照试验。试验结果显示,与使用安慰剂的患者相比,Adquey能显著帮助更多轻中度特应性皮炎患者在四周后达到皮肤完全或几乎完全清除的目标,即研究者总体评估(IGA)成功。在针对15至70岁人群的试验中,使用Adquey的患者中有约38.5%在第四周达到IGA成功目标,安慰剂组仅为12.6%;在针对2至14岁儿童的研究中,Adquey组有47.1%的患者达到该目标,安慰剂组仅为18.1%。儿童患者在湿疹面积和严重程度指数方面也表现出更显著的改善,且疗效最早在第一周即可显现。
该药物的安全性特征在所有试验中保持一致,研究中的副作用大多为轻度至中度。最常见的不良反应为鼻咽炎,发生率为6%。较少见的不良反应(发生率低于1%)包括用药部位毛囊炎、接触性皮炎、用药部位皮疹和传染性软疣。
Adquey的活性成分地法米司特由大冢制药发现和开发,自2021年起已在美国授权给Acrotech公司,为美国特应性皮炎患者提供了一种非类固醇类的新治疗选择。

注:以上资讯来源于网络,并由致泰药业整理编辑(如有错漏,请帮忙指正),只为提供全球最新上市药品的资讯,帮助全球各地华人患者了解国际新药动态,仅供医护人员内部讨论,不作任何用药建议及依据, 如想要进一步了解药品,请咨询主治医师。