四大王牌抗癌药:Opdivo/Keytruda/Yervoy /Tecentriq
本文介绍了4种PD-1/PD-L1药物:Opdivo纳武单抗、Yervoy易普利姆玛、Keytruda派姆单抗和Tecentriq阿特珠单抗,具有强有力的竞争优势,被誉为抗癌药界的四大王牌。目前这类药物在进行的临床试验时,入组的患者是否需要对PD-1表达进行筛选引起了人们进一步探讨。进一步积累的临床结果将决定这些药物中哪个会在IO市场上走得更远。
小野制药和百时美施贵宝(BMS)合作开发的Opdivo (nivolumab)是作用于T细胞、祖B细胞和巨噬细胞表面受体PD-1(程序细胞死亡蛋白1)的抑制剂,近来在肿瘤免疫(IO)治疗中有积极的临床试验结果。PD-1及其配体PD-L1和2(程序细胞死亡1配体1和2)在免疫系统中起着抑制T细胞活化的作用。
此类治疗性单抗通过抑制肿瘤PD-1的表达,使免疫系统攻击肿瘤细胞从而对抗多种肿瘤,频频出现在各大临床肿瘤学会的聚光灯下。
1、 Opdivo:2020年销售额预计:67.46亿美元
以上图片为Opdivo纳武单抗100毫克在致泰药业实拍图
【英文商品名】Opdivo
【英文药品名】Nivolumab
【中文药品名】纳武单抗
【生产厂家名】BMS
用于黑色素瘤
以上图片为Opdivo纳武单抗40毫克在致泰药业实拍图
Opdivo于2014年在日本获批上市,用于不可切除的黑色素瘤。接着于2015年在美国上市,除了用于不可切除的黑色素瘤患者,还可用于Yervoy(ipilimumab,BMS的另一个免疫检查点抑制剂)治疗后进展的黑色素瘤,或BRAF V600突变阳性患者BRAF抑制剂治疗后进展的黑色素瘤。
2、Keytruda:2020年销售额预计:39.22亿美元
以上图片为Keytruda派姆单抗100毫克在致泰药业实拍图
派姆单抗 Keytruda
【英文商品名】Keytruda
【英文药品名】Pembrolizumab
【中文药品名】派姆单抗
【生产厂家名】默沙东
默沙东的PD-1抑制剂单抗Keytruda(pembrolizumab)于2014年在美国上市,获批的适应症和Opdivo一样用于不可切除或转移的黑色素瘤,在ASCO年会也佔据了一席之地。2015年3月,该药物基于Ⅰ期KEYNOTE-001(NCT01295827)临床试验在实体瘤的数据,通过「早期药物上市计划」在英国以同样的适应症上市。该上市方案基于2014年6月的MAA申请,且在2015年5月EMA的CHMP也支持该药物用于一二线治疗晚期(不可切除或转移性)黑色素瘤患者。
在未经Yervoy治疗或Yervoy治疗后复发的转移性黑色素瘤患者中,总缓解率分别为40%和28%。Keytruda用于NSCLC治疗的首个临床数据也在此次会议上公佈。
2015年6月,FDA接受了该药物用于铂类化疗方案(或者存在EFGR或ALK突变,FDA已批淮的相应治疗药物)治疗中或治疗后进展的晚期NSCLC适应症的补充申请。
在肿瘤报告会议上,默沙东公佈了Keytruda用于多种肿瘤的临床数据,包括用于PD-1阳性的晚期小细胞肺癌、食管癌和卵巢癌的Ⅰb期临床KEYNOTE-028 (NCT02054806)的初步数据。
值得一提的是,在一项用于经既往治疗并进展的转移性肿瘤患者的Ⅱ期临床试验中(NCT01876511),研究者分析了PD-1抑制与DNA错配修复缺陷的关系。在MMR缺陷的结直肠癌患者(CRC)和MMR-缺陷的非CRC患者中,首要终点客观缓解率分别为62%和60%,而在MMR完全的CRC患者中为0%。同样,MMR缺陷的患者疾病控制率也高。之前研究者曾注意到高突变发生和对于PD-1抑制剂的响应正相关,因此假定有一部分的肿瘤患者对免疫检查点抑制剂更加敏感。这一研究结果刚好验证了之前的假设。
接着这一研究,默沙东又开展了在转移性CRC患者中的KEYNOTE 164 (NCT02460198)临床试验。分析师一致预测该药物销售额将从2015年的5.06亿美元增长到2020年的39.22亿美元。
3、Yervoy 易普利姆玛注射液 预计2020年销售额:23.77亿美元
以上图片为Yervoy易普利姆玛50毫克在致泰药业实拍图
Yervoy通过阻断T细胞表面CTLA-4(细胞毒T淋巴细胞相关蛋白4)受体活化,防止抑制信号传导给T细胞。与PD-1检查点抑制剂类似,CTLA-4检查点抑制剂通过阻止肿瘤细胞逃逸起作用。
在今年的肿瘤报告会议上,Ⅲ期临床试验CheckMate 067 (NCT01844505)结果发佈是最精彩的报告之一。试验共入组945例未经治疗的晚期黑色素瘤患者,对比联合Opdivo/Yervoy给药4次与两药单用给药4次(採用同样的包含安慰剂的替代给药方案)的总生存期和无进展生存期(PFS)。结果显示,在意向治疗的人群中,随访期不少于9个月,联用组的中位PFS(11.5个月)较使用Opdivo(6.9个月)或Yervoy(2.9个月)单药治疗的均显著延长。联用组的客观缓解率也较单药显著提升(57.6%vs43.7%vs19%)。
2015年2季度,FDA通过了Opdivo的两个优先审评申请:一是单药用于此前未接受治疗的不可切除或转移黑色素瘤,二是联用Opdivo和Yervoy用于未经治疗的晚期黑色素瘤。PDUFA日期分别为2015年8月和9月。因此,今年是成为BMS在IO领域又一个重要的注册年份。分析师预测Opdivo将从2015年的7.24亿美元销售增长到2020年的67.46亿美元。
然而,CheckMate 067临床结果中联用组的安全性问题引起分析师们的争议。ASCO专家Steven O』Day认为这将「抵消该药给一些患者带来的益处」。在该临床试验中,联用组中与药物相关的严重不良反应发生率为55%,其中有36.4%患者因此停药。在Ⅱ期CheckMate 069 (NCT01927419)试验中,儘管Opdivo和Yervoy联用得到了很好的总缓解率(60%),但不良反应发生率51.1%也是非常高的。而在单用Yervoy的试验组,总缓解率为11%,治疗相关不良反应发生率为19.6%。
4、Tecentriq atezolizumab 阿特珠单抗 2020年销售额预计:23.26亿美元
IO领域另一个值得关注的PD-检查点抑制剂是罗氏的PD-L1抑制剂atezolizumab,该药于2015年4月开始Ⅲ期临床,用于经PD-L1选择的未经化疗的Ⅳ期NSCLC患者,与顺铂(或卡铂)联用培美曲塞对照(NCT02409342),或者与顺铂(或卡铂)联用吉西他滨对照(NCT02409355)。之前一项在563名NSCLC患者的研究中,atezolizumab的总反应率为20%,而且在保存的组织中PD-L1的表达和对抗PD-L1的治疗响应也呈现了一定的相关性。在PD-L1表达高的患者中观察到了最佳缓解率(50%)。分析师一致预测该药物销售额将从2016年的1.16亿美元增长到2020年的23.26亿美元。
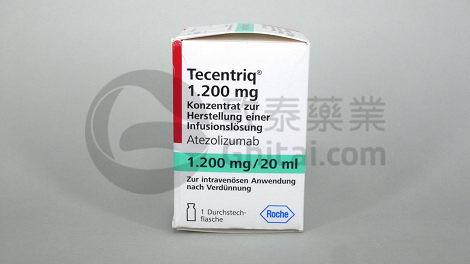
以上图片为Tecentriq阿特珠单抗1200毫克在致泰药业实拍图
进一步积累的临床结果将决定这些药物中哪个会在IO市场上走得更远。由于需要进行PD-L1选择性研究,并且联用带来副作用增加等制约因素,进一步的临床研究也将决定这些药物未来是否会成功,是否还是会被新的肿瘤治疗手段所取代。
Opdivo纳武单抗、Yervoy易普利姆玛、Keytruda派姆单抗和Tecentriq阿特珠单抗目前仍未在中国大陆上市, 海外客户如需要更多资讯, 欢迎与致泰药业联络查询。香港致泰药业是经香港政府卫生署注册的药品批发商,专注于全球新特药品进出口业务。


