欧盟批准Dupixent(度普利尤单抗)用于儿童慢性自发性荨麻疹治疗
2026年4月13日,欧盟委员会批准了Dupixent(dupilumab,达必妥/度普利尤单抗)用于治疗2至11岁中重度慢性自发性荨麻疹儿童患者,这些患者对组胺H1拮抗剂治疗反应不佳,且未接受过针对慢性自发性荨麻疹的抗免疫球蛋白E治疗。此次获批扩大了Dupixent在欧盟的慢性自发性荨麻疹适应症范围,此前该药品已获批用于12岁及以上成人和青少年的慢性自发性荨麻疹治疗,此次获批后,Dupixent成为欧盟首个用于治疗2至11岁该病症儿童患者的靶向药物。
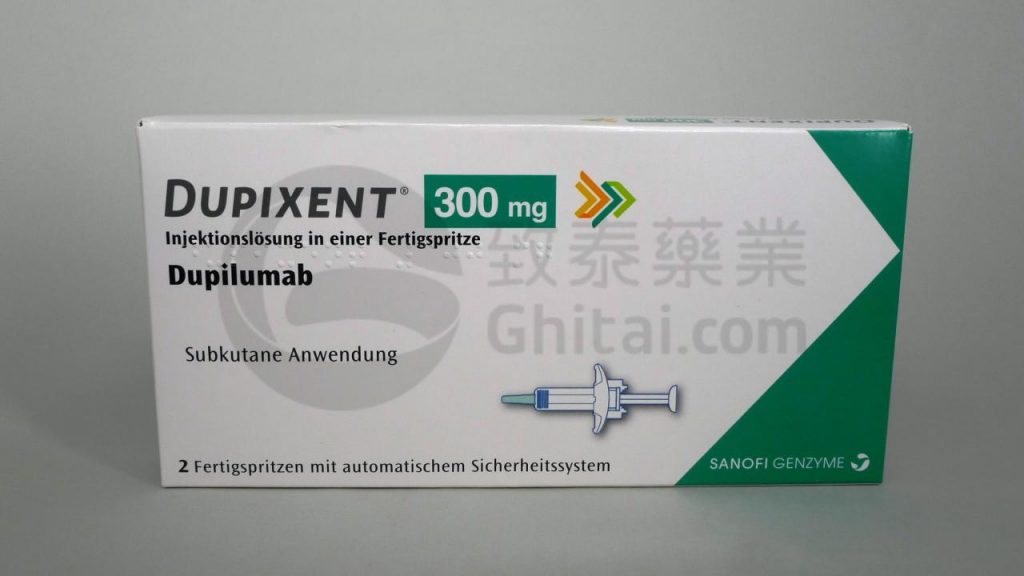
以上图片为Dupixent(dupilumab,度普利尤单抗)在致泰药业实拍图
Dupixent的活性成分为度普利尤单抗,其作用机制是抑制白细胞介素4和白细胞介素13的信号传导,这两种细胞因子是2型炎症的关键核心驱动因子,而慢性自发性荨麻疹作为一种慢性炎症性皮肤病,其发病与2型炎症密切相关,因此Dupixent通过针对性抑制相关信号传导,为儿童慢性自发性荨麻疹提供了一种全新的靶向治疗方案。该药品为皮下注射剂,通常可在大腿或腹部进行注射,剂型包括预充式笔或注射器,方便使用。
此次欧盟获批的依据来自LIBERTY-CUPID临床试验项目的数据,该项目包括两项针对成人的3期临床试验和一项针对2至11岁儿童的单臂3期CUPID Kids临床试验。其中,两项成人3期临床试验的疗效数据经过外推,结合儿童临床试验中的药代动力学、安全性和疗效数据,共同支撑了此次获批。两项成人3期临床试验共纳入284名12岁及以上对组胺H1拮抗剂治疗反应不佳且未接受过抗免疫球蛋白E治疗的慢性自发性荨麻疹患者,患者基线时7天瘙痒严重程度评分平均为15至16分,7天荨麻疹活动评分平均为28.2至31.4分。
临床试验结果显示,在治疗24周时,与安慰剂相比,Dupixent显著降低了患者的荨麻疹活动度,包括瘙痒和荨麻疹严重程度的综合指标。其中一项成人试验中,Dupixent组患者7天瘙痒严重程度评分较基线降低10.44分,安慰剂组降低6.02分;7天荨麻疹活动评分较基线降低20.99分,安慰剂组降低11.95分;47%的Dupixent组患者达到疾病良好控制状态,安慰剂组为24%;32%的Dupixent组患者实现完全缓解,安慰剂组为13%。另一项成人试验中,Dupixent组患者7天瘙痒严重程度评分较基线降低8.50分,安慰剂组降低6.13分;7天荨麻疹活动评分较基线降低15.61分,安慰剂组降低11.27分;40%的Dupixent组患者达到疾病良好控制状态,安慰剂组为23%;30%的Dupixent组患者实现完全缓解,安慰剂组为17%。
安全性方面,来自成人临床试验和儿童CUPID Kids临床试验的数据显示,Dupixent的安全性特征与该药品在已获批皮肤科适应症中的已知安全性特征基本一致。治疗期间出现的不良事件发生率在Dupixent组和安慰剂组中均为53%,其中Dupixent组较安慰剂组更常见的不良事件(发生率≥5%)为注射部位反应,发生率为12%,安慰剂组为4%。此外,Dupixent在慢性自发性荨麻疹患者中观察到的其他常见不良事件还包括关节痛、结膜炎、视力模糊、疱疹病毒感染和角膜炎等,发生率均≥2%。
此次获批后,Dupixent在欧盟已获批用于四种慢性疾病的12岁以下儿童治疗,均与2型炎症相关。欧盟人用药品委员会曾于2026年2月26日就Dupixent扩大适应症给出积极意见,推荐扩展其慢性自发性荨麻疹适应症至2至11岁儿童,此次欧盟委员会的批准正式落实了这一推荐。更新后的药品说明书将详细载明该适应症的使用建议,将在欧盟委员会做出批准决定后,以欧盟所有官方语言发布在欧洲药品管理局网站上。

注:以上资讯来源于网络,并由致泰药业整理编辑(如有错漏,请帮忙指正),只为提供全球最新上市药品的资讯,帮助全球各地华人患者了解国际新药动态,仅供医护人员内部讨论,不作任何用药建议及依据, 如想要进一步了解药品,请咨询主治医师。