中重度斑块型银屑病治疗药物Bimzelx(比美吉珠单抗)在美国上市
在医学领域的不断创新中,全球生物制药公司优时比(UCB)于11月14日宣布了一项引人瞩目的消息——Bimzelx(bimekizumab-bkzx,比美吉珠单抗)已在美国成功上市。这一突破性的治疗药物针对中度至重度斑块型银屑病,为患者提供了一种新的治疗选择。本文将深入探讨Bimzelx的特点、机制以及基于临床试验的疗效和安全性。
目录
Bimzelx的突破性特点
靶向治疗机制
Bimzelx通过皮下注射给药,是一种新型人源化单克隆IgG1抗体。其设计目标是阻断白细胞介素17A(IL-17A)和白细胞介素17F(IL-17F)这两种信号蛋白,这些蛋白负责推动斑块型银屑病中的炎症反应。与其他生物药物不同,Bimzelx是首个选择性抑制这两种细胞因子在银屑病治疗中发挥作用的方法。
个性化治疗方案
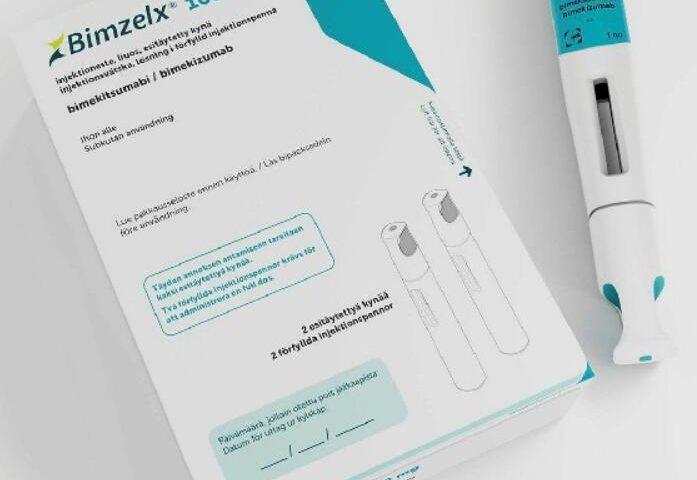
Bimzelx提供了单剂量预填充自动注射器或预填充注射器,含160mg/mL溶液。这种创新的治疗方式使得患者在接受医疗服务提供者的皮下注射培训后能够自行注射Bimzelx,增加了治疗的便捷性和个性化。
临床试验的基础和疗效评估
试验设计
Bimzelx的批准基于3期BE VIVID(NCT03370133)、BE READY(NCT03410992)和BE SURE(NCT03412747)试验的数据。这些试验共涵盖了1480名患有中度至重度斑块状银屑病的成年人。试验的设计主要关注了两个主要终点:研究者整体评估(IGA)评分为0(“清除”)或1(“几乎清除”)且与初始相比至少有2级改善的患者比例,以及相对于初始银屑病面积和严重程度指数90 (PASI 90)缓解至少降低90%的患者比例。
疗效评估
在3期试验中,Bimzelx展现了其在与安慰剂或常用药物阿达木单抗和乌司奴单抗相比实现更好的皮肤清除率。根据银屑病面积和严重程度指数(PASI)或研究者评估,在所有研究中,85%至91%的Bimzelx治疗的患者在第16周获得了症状清除或几乎清除的皮肤。此外,根据公司提供的数据,在所有研究中,59%~68%的患者在第16周时实现了皮肤症状完全清除(或PASI 100)。
安全性评估
Bimzelx的上市伴随着对其安全性的深入研究。观察到的最常见不良反应包括上呼吸道感染、口腔念珠菌病、头痛、注射部位反应、癣感染、胃肠炎、单纯疱疹感染、痤疮、毛囊炎、其他念珠菌感染和疲劳。此外,Bimzelx的处方信息中包括与自杀意念和行为、结核病、肝脏生化异常和炎症性肠病相关的风险。
总体来讲,Bimzelx的成功上市为中度至重度斑块型银屑病的患者带来了新的曙光。其革命性的治疗机制和独特的个性化治疗方案展现了医学领域不断创新的力量。随着更多患者在实际治疗中获得显著的皮肤改善,Bimzelx的出现为改善患者生活质量提供了有力的支持。我们期待着进一步的临床观察和未来更多创新治疗的崛起,以满足患者不断增长的医疗需求。

注:以上资讯来源于网络,并由致泰药业整理编辑(如有错漏,请帮忙指正),只为提供全球最新上市药品的资讯,帮助全球各地华人患者了解国际新药动态,仅供医护人员内部讨论,不作任何用药建议及依据, 如想要进一步了解药品,请咨询主治医师。