10
7月
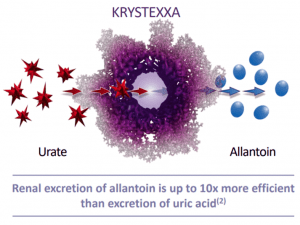
KRYSTEXXA®(pegloticase)注射甲氨蝶呤的 MIRROR 随机对照试验的长期数据发表在 ACR Open Rheumatology 上
都柏林,2023 年 7 月 6 日–(美国商业资讯)–Horizon Therapeutics plc(纳斯达克股票代码:HZNP)今天宣布公布 KRYSTEXXA ®(pegloticase)注射液甲氨蝶呤的 MIRROR 随机对照临床试验的长期数据。ACR 开放风湿病学中常用的免疫调节剂。作者兼主任 Kenneth Saag 医学博士说:“这些 12 个月数据的发布强化了第 6 个月显示的关键发现,包括降尿酸反应的持久性、输注反应的减少以及聚乙二醇酶与甲氨蝶呤联合给药时的免疫原性降低。”阿拉巴马大学伯明翰分校临床免疫学和风湿病学博士。“令人鼓舞的是,随着时间的... 查看详情
10
7月
焦点——几乎没有痛风管道爆发的迹象
亚洲开发商在生物制药的痛风产品管线中占据主导地位,其中 Selecta 和 Sobi 的 SEL-212 成为罕见的全球重点项目。长期以来,痛风一直困扰着药物开发商,但本周,这种疾病因另一个原因而成为人们关注的焦点。FTC指出 Krystexxa 的垄断地位是其不愿批准安进收购该药物所有者 Horizon 的一个原因。 对管道的观察为这一立场提供了一些支持。只有一个项目可能很快会在慢性痛风治疗中挑战 Krystexxa:Selecta 和瑞典 Orphan Biovitrum 的 SEL-212,该项目将于明年向监管机构提交申请。除此之外,研究主要是由亚洲开发商进行的,他们运行以区域为重点... 查看详情
09
7月
AACR:三个关键基因的突变与 KRAS G12C 抑制剂治疗的肺癌患者不良预后相关
佛罗里达州奥兰多——德克萨斯大学 MD 安德森癌症中心的研究人员领导的一项新研究发现,三种肿瘤抑制基因(KEAP1、SMARCA4 和 CDKN2A)同时发生的突变与 KRAS G12C 患者的不良临床结果有关。使用 KRAS G12C 抑制剂阿达格拉西 (adagrasib) 或索托拉西 (sotorasib) 治疗的突变型非小细胞肺癌 (NSCLC)。 该研究结果今天在美国癌症研究协会 (AACR) 2023 年年会上公布,并发表在AACR 期刊《Cancer Discovery》上。这项研究涵盖了迄今为止使用任一药物治疗的 KRAS G12C 突变 NSCLC 患者的最大队列,为临床医生... 查看详情
09
7月
礼来公司通过 AACR 数据发布寻求一线 KRAS 治疗
礼来公司在奥兰多举行的美国癌症研究协会 (AACR) 会议上公布了其 KRAS G12 抑制剂的首个临床数据。礼来公司的研究人员表示,他们希望通过使其成为第一个获得批准作为一线治疗药物的药物,从而将其 I 期候选药物与竞争激烈的 KRAS 领域区分开来。 目前批准的竞争对手作为二线治疗。KRAS G12 是 KRAS 癌基因中的一种特定基因突变。KRAS 基因产生一种称为 K-Ras 的蛋白质,有助于调节细胞生长和分裂。KRAS 基因的突变可能导致产生一种有缺陷的 K-Ras 蛋白,该蛋白始终处于活跃状态,导致细胞不受控制地生长和分裂,从而导致癌症。KRAS G12 突变明确指的是 KRAS ... 查看详情
08
7月
KRAZATI™(adagrasib)现已从 Onco360 上市,用于治疗 KRAS G12C 突变的局部晚期或转移性非小细胞肺癌 (NSCLC) 成年患者
肯塔基州路易斯维尔–(美国商业资讯)–美国领先的独立专业药房Onco360 ®已被Mirati Therapeutics选为KRAZATI ® (adagrasib)的专业药房合作伙伴,KRAZATI ® (adagrasib)是一种RAS GTPase家族抑制剂适用于治疗经 FDA 批准的测试确定患有 KRAS G12C 突变的局部晚期或转移性非小细胞肺癌 (NSCLC) 的成年患者,这些患者之前至少接受过一种全身治疗。该适应症根据客观缓解率(ORR)和缓解持续时间(DOR)在加速批准下获得批准。该适应症的继续批准可能取决于验证性试验中临床益处的验证。 Onco360... 查看详情
08
7月
NCCN 推荐 Krazati 用于治疗胰腺癌亚群
美国国家综合癌症网络 (NCCN) 现推荐 Krazati(adagrasib)用于治疗 KRAS G12 突变胰腺癌患者。“NCCN 指南是任何医学领域最全面、更新最频繁的临床实践指南,更新旨在反映癌症研究和管理领域的快速进步,”该系副教授 Shubham Pant 博士说。胃肠道医学肿瘤学与德克萨斯大学 MD 安德森癌症中心癌症治疗研究部门联合任命,在接受 CURE® 采访时表示,并指出 NCCN 推荐的药物更有可能包含在健康保险范围内。Pant 向 CURE 概述了 Krazati 在这部分患者中的使用情况,以及该药物背后有前景的研究。您能否介绍一下使用 Krazati 治疗 KRAS ... 查看详情
07
7月
癌症日益成为一种慢性疾病
(Keystone-ATS)癌症正在成为一种慢性但不那么致命的疾病,目前估计价值数千亿美元的世界抗癌药物市场将进一步扩大。财富管理公司 Candriam 的肿瘤学和生物技术基金经理 Rudi Van den Eynde 表示。这位专家在瑞士财经门户网站Cash发表的采访中表示,“全球肿瘤药物市场价值约2000亿美元”。“这不仅是医疗保健市场中最大的领域,而且预计未来几年的增长也是最高的。”这位专家解释说,癌症是一种由于世界人口老龄化而导致患者数量不断增加的疾病。“一般来说,你从 60 岁开始就会生病。但结直肠癌和乳腺癌除外,这些癌症的患者似乎越来越年轻。” 在该领域经营的公司可以做得很好。“药... 查看详情
07
7月
Mirati 的 Krazati 对未经治疗的 KRAS 突变非小细胞肺癌脑转移患者显示出疗效
纽约 – Mirati Therapeutics 希望根据 Krazati(adagrasib)在 KRAS G12C 突变非小细胞肺癌未经治疗的中枢神经系统(CNS)转移患者中的阳性数据读数,为 KRAS 抑制剂的颅内疗效设定标准。研究人员本月早些时候在《临床肿瘤学杂志》上发表了 I/II 期 KRYSTAL-1 试验中 19 名可评估的晚期或转移性 KRAS G12C 突变 NSCLC 患者的前瞻性疗效和生存数据,这些患者患有神经系统稳定、无症状、未经治疗的 CNS 转移 。这些发现增强了 Mirati 推进 Krazati 其他研究的信心,包括一项评估该药物在患有未经治疗的脑转移的 NS... 查看详情
06
7月
Alnylam 的第二种淀粉样变性疗法获得 FDA 批准
在 FDA 批准第一种治疗罕见疾病遗传性 ATTR 淀粉样变性的药物四年后,Alnylam 又获得了第二种药物 Amvuttra 的批准,该药物具有更简单、更适合患者的给药方案。ATTR 淀粉样变性是一种侵袭性、快速进展、使人衰弱和致命的疾病,Alnylam 于 2018 年推出的早期Onpattro (patisiran) 用于治疗与该疾病相关的多发性神经病,这对患者来说是向前迈出的一大步。 Amvuttra (vutrisiran) 也已被批准用于治疗 ATTR 多发性神经病,但 Onpattro 每三周静脉注射一次,而新药则每三个月皮下注射一次。这使其与 Onpattro 和 Ionis... 查看详情
06
7月
NICE 推荐 Alnylam 的 RNAi 疗法用于治疗遗传性淀粉样变性
RNA 干扰 (RNAi) 治疗公司宣布,Alnylam Pharmaceuticals 的 Amvuttra (vutrisiran) 已被国家健康与护理卓越研究所 (NICE) 推荐作为治疗遗传性淀粉样变性的一种选择。 NICE 的决定使 Amvuttra 成为首批在其简化的试点流程下获得积极建议草案的罕见病药物之一,该流程旨在加速患者获得有前途的新疗法。 根据最终指导,英国患有遗传性转甲状腺素蛋白相关 (ATTR) 淀粉样变性的患者将可以选择 Amvuttra,每三个月进行一次皮下注射,而现有疗法需要每几周或更频繁地注射一次。 该公司表示,预计该指南将适时在威尔士实施。ATTR 淀粉样变... 查看详情