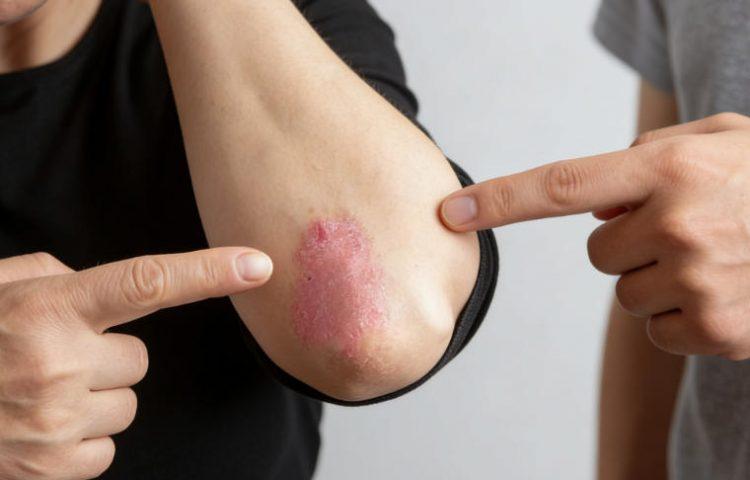
美国FDA批准ICOTYDE(Icotrokinra)用于中重度斑块状银屑病治疗
2026年3月18日,强生公司宣布,美国食品药品监督管理局已批准ICOTYDE(Icotrokinra)用于治疗中重度斑块状银屑病。该药物适用于12岁及以上、体重至少40公斤、适合接受系统治疗或光疗的成人和儿科患者。
ICOTYDE是全球首个也是唯一一款靶向白细胞介素-23受体的口服肽类药物,通过选择性结合并阻断白细胞介素-23受体发挥作用,该受体是斑块状银屑病炎症信号传导的关键通路。其剂型为每日一次的口服药片,为那些经局部治疗未能获得足够疾病控制、需要系统治疗的患者提供了一种新的治疗选择。
该药物的获批基于ICONIC临床开发项目的四项III期试验数据,共纳入2500名患者,试验同时评估了该药物在成人、青少年患者中的疗效,以及在头皮、生殖器等高危部位银屑病的治疗效果,并包含与活性对照药物的头对头试验。
在头对头优效性研究中,约70%的患者在第16周时达到皮肤清除或几乎清除状态,55%的患者达到银屑病面积和严重程度指数90缓解反应,即病情改善超过90%。在一项包含684名受试者的随机、双盲、安慰剂对照III期试验中,456名受试者接受每日200毫克ICOTYDE治疗,228名接受安慰剂治疗,第16周时,ICOTYDE治疗组65%的受试者达到研究者总体评估0/1反应,安慰剂组为8%;ICOTYDE治疗组50%的受试者达到银屑病面积和严重程度指数90缓解反应,安慰剂组为4%,两项对比差异均具有统计学意义。此外,ICOTYDE治疗组33%的受试者达到皮肤完全清除,安慰剂组为1%;27%的受试者达到银屑病面积和严重程度指数100缓解反应,安慰剂组不足1%,差异均具有统计学意义。
安全性方面,截至第16周,ICOTYDE治疗组的不良反应发生率与安慰剂组相差仅1.1%以内,两组均有49%的受试者报告至少一次不良反应,最常见的不良反应包括鼻咽炎、上呼吸道感染、头痛、恶心、咳嗽、疲劳和真菌感染。截至第52周,未发现新的安全信号,且不良反应的暴露调整发生率在第24周内保持稳定。处方信息提示,该药物可能与感染相关,需监测患者的感染迹象,包括结核病。
ICOTYDE由强生公司与Protagonist Therapeutics合作开发,强生公司拥有该药物全球范围内2期临床试验及以后阶段的开发权,以及针对广泛适应症的商业化权利。目前,该药物除用于中重度斑块状银屑病外,还在活性银屑病关节炎、中重度活动性溃疡性结肠炎和中重度活动性克罗恩病等其他疾病领域进行研究。

注:以上资讯来源于网络,并由致泰药业整理编辑(如有错漏,请帮忙指正),只为提供全球最新上市药品的资讯,帮助全球各地华人患者了解国际新药动态,仅供医护人员内部讨论,不作任何用药建议及依据, 如想要进一步了解药品,请咨询主治医师。