13
4月
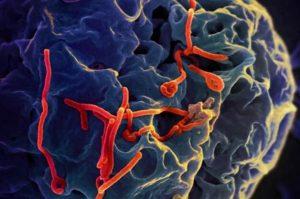
FDA批准SuVax™用于预防和暴露后预防苏丹埃博拉病毒感染的孤儿药资格
在当前全球疫情不断肆虐的背景下,针对致命疾病的疫苗研发显得尤为紧迫而重要。近日,美国食品和药物管理局(FDA)的一项重要决定再次将人们的目光聚焦在疫苗领域。Soligenix, Inc.(以下简称Soligenix)宣布,其新型疫苗SuVax™已获得FDA的孤儿药资格,这标志着在预防和暴露后预防苏丹埃博拉病毒感染方面迈出了重要一步。 SuVax™药物资格获批 2024年4月11日,Soligenix公司宣布其针对苏丹埃博拉病毒(SUDV)的疫苗SuVax™已被FDA孤儿产品开发办公室授予孤儿药称号。这一称号意味着SuVax™的活性成分,即重组表达的SUDV亚单位蛋白疫苗糖蛋白,被认可用于预防S... 查看详情
12
4月
FDA授予LYT-200用于复发/转移性头颈部鳞状细胞癌的快速通道资格
在癌症治疗领域,迅速发展的科技和新药物的出现给患者带来了新的希望。近期,美国食品药品监督管理局(FDA)授予了一项重要的药物快速通道设计,这将有望改善头颈部鳞状细胞癌(HNSCC)患者的治疗前景。具体来说,是针对头颈部鳞状细胞癌的一种全新的单克隆抗体LYT-200获得了FDA的快速通道设计。 LYT-200药物的重要性 LYT-200是一种针对特定肿瘤驱动因子和免疫抑制剂半乳糖凝集素-9(galectin-9)的全人源单克隆抗体。通过针对galectin-9,LYT-200有望在治疗HNSCC等恶性肿瘤方面发挥重要作用。据纯技健康(PureTech Health)宣布,FDA已经授予LYT-2... 查看详情
12
4月
FDA授予CAN-2409(aglatimagene besadenovec)治疗胰腺癌孤儿药资格
FDA已经向多模式生物免疫治疗候选药物aglatimagene besadenovec(CAN-2409)授予了孤儿药物认定,用于治疗胰腺癌患者。 胰腺癌是一种具有高度侵袭性的癌症,常常在早期没有明显症状,导致患者往往在确诊时已经晚期。目前的治疗手段效果有限,对患者生存率的提高至关重要。因此,获得FDA孤儿药物认定的CAN-2409带来了新的曙光,为胰腺癌患者带来了治疗上的希望。 CAN-2409在临床试验中的表现 2024年4月4日,Candel Therapeutics宣布了CAN-2409在与瓦拉西克洛韦和标准治疗联合应用后的临床试验PaTK02(NCT02446093)的中期结果。该试... 查看详情
12
4月
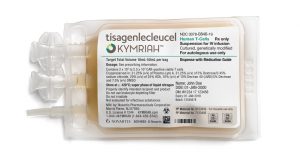
英国NICE推荐Kymriah(Tisagenlecleucel)用于儿童复发难治性B细胞急性淋巴细胞白血病
英国国家卫生与医疗卓越研究所(NICE)日前推荐了Kymriah(Tisagenlecleucel)用于治疗儿童和年轻成人B细胞急性淋巴细胞白血病(B-ALL)的新指南,这一决定将影响到一批不符合标准治疗条件的患者,为他们带来新的治疗希望。 NICE推荐背景 英国NICE推荐了Kymriah(Tisagenlecleucel)用于治疗儿童和年轻成人25岁及以下的B-ALL患者,这些患者在治疗后没有反应、在干细胞移植后复发,或者复发两次或更多次。这一推荐意味着Kymriah(Tisagenlecleucel)将从英国国家卫生服务(NHS)癌症药物基金(CDF)的临床试用阶段进入常规使用阶段。 临... 查看详情
12
4月
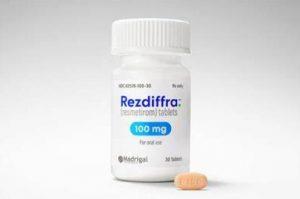
非酒精性脂肪性肝炎新药Rezdiffra(resmetirom)在美国市场上市
在医学领域,随着科学技术的不断进步,我们见证了一项新的里程碑之作——非酒精性脂肪性肝炎(NASH)的突破性治疗药物Rezdiffra(resmetirom)近日在美国成功上市。这不仅标志着医学界对于这一肝脏疾病的认知和治疗手段迈出了一大步,更为数百万患者带来了新的希望和机遇。 Rezdiffra(resmetirom)是一种口服甲状腺激素受体(THR)-β选择性激动剂,它的上市填补了NASH治疗领域的空白。根据最新的数据显示,Rezdiffra可用于治疗成人非肝硬化中度至晚期肝纤维化(与F2至F3期纤维化一致)的患者。这一突破性药物的问世,为那些饱受NASH之苦的患者带来了新的曙光。 临床试验... 查看详情
11
4月
SMC接受玛伐凯泰Camzyos(mavacamten)用于梗阻性肥厚型心肌病的辅助治疗选择
近日,苏格兰药物委员会(Scottish Medicines Consortium,SMC)宣布接受了一种名为Camzyos®(Mavacamten,玛伐凯泰)的药物,作为成人合并症状性梗阻性肥厚型心肌病(HCM)的辅助治疗选项,可在英国国民保健服务(NHS)中使用。这一消息将对患有这一疾病的患者产生深远影响,有望改善他们的生活质量。 苏格兰药物委员会接受玛伐凯泰作为肥厚型心肌病治疗方案 肥厚型心肌病是一种常见的遗传性心脏病,影响着英国约500人中的一人。近日,苏格兰药物委员会宣布接受了一种名为Camzyos®(Mavacamten,玛伐凯泰)的药物,作为成人合并症状性梗阻性肥厚型心肌病(HC... 查看详情
11
4月
FDA授予他米巴罗汀(Tamibarotene)用于新诊断的急性髓系白血病的快速通道资格
急性髓系白血病(AML)是一种严重的血液疾病,尤其是对于年长患者而言。近年来,随着基因组学和分子生物学的进步,我们对AML的治疗有了更深入的理解,也为新疗法的开发提供了机会。在这个背景下,美国食品药品监督管理局(FDA)的快速跟踪认证对于AML患者的治疗意义重大。 他米巴罗汀(Tamibarotene)在新诊断AML中获得FDA快速跟踪认证 据Syros Pharmaceuticals发布的新闻稿称,FDA已经授予了他米巴罗汀(Tamibarotene)在新诊断急性髓系白血病(AML)患者中的快速跟踪认证,特别是对于年龄在75岁及以上、携带RARA基因过度表达的患者,而这一过度表达是通过FDA... 查看详情
11
4月
FDA授予LSTA1(CEND-1)治疗骨肉瘤的孤儿药资格
近日,美国食品药品监督管理局(FDA)已正式授予LSTA1(CEND-1)孤儿药物认定,用于治疗骨肉瘤患者,这一消息为肿瘤患者带来了新的曙光。 LSTA1的作用机制和研究背景 LSTA1是一种新型药物,利用肿瘤细胞内的一种新颖摄取途径,使共价结合的抗癌药物能够更有效地渗透实体肿瘤并在肿瘤环境中积聚。这一机制是通过LSTA1与α-v整合素的结合实现的,后者在肿瘤中选择性表达,而在健康组织中则不存在。在结合后,LSTA1被蛋白酶切割,形成CendR片段,然后结合到神经丝素1上,启动并激活肿瘤细胞内的摄取途径。这一靶向过程使得药物能够更好地渗透肿瘤细胞并在其中积聚,从而增强其在实体肿瘤中的疗效。 L... 查看详情
11
4月
依拉米肽(Elamipretide)治疗Barth综合征已提交FDA审查
Barth综合征是一种罕见而严重的遗传性疾病,由于线粒体心磷脂缺乏而引起,其主要特征包括肌肉无力和心脏异常,往往导致心力衰竭、反复感染、生长延迟以及预期寿命缩短。然而,迄今为止,针对这一疾病的治疗方法非常有限,缺乏获得FDA或EMA批准的药物。因此,针对Barth综合征的新药研发备受期待。 新药申请进展 最近,Stealth BioTherapeutics公司宣布,其新药Elamipretide(依拉米肽)已经提交给美国FDA进行审查,用于治疗Barth综合征。这一消息意味着FDA已接受该药物的新药申请(NDA),并计划召开一次咨询委员会会议来讨论该申请。值得一提的是,该申请被指定为标准审查,... 查看详情
10
4月
FDA授予PT217用于广泛期小细胞肺癌的快速通道资格
肺癌一直是全球范围内最为常见的癌症之一,而广泛期小细胞肺癌(Extensive Stage Small Cell Lung Cancer, ES-SCLC)更是其中最具挑战性的类型之一。对于此类患者,药物治疗的需求亟待满足。然而,近期的一项重要决定或许将为这一领域带来新的希望。 PT217获FDA快速通道认定 近日,美国食品药品监督管理局(FDA)已将PT217授予快速通道认定,以治疗广泛期小细胞肺癌(ES-SCLC)患者。 PT217是一种首创的天然IgG样双特异性抗体,针对DLL3和CD47,目前正在进行I期SKYBRIDGE试验(NCT05652686),用于治疗SCLC、大细胞神经内分... 查看详情