22
9月
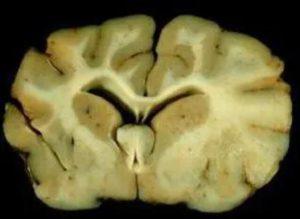
FDA接受OTL-200在异染性脑白质营养不良中的生物制品许可证申请并获得优先审查
近日,全球基因疗法领导者Orchard Therapeutics(Nasdaq:ORTX)宣布,美国食品和药物管理局(FDA)已接受其OTL-200在异染性脑白质营养不良(MLD)治疗方面的生物制品许可申请(BLA),并予以优先审查。 FDA已经设定了截止日期,PDUFA目标日期为2024年3月18日。 “对于长期以来一直遭受这种毁灭性而残酷疾病影响的美国患者和家庭来说,今天是向前迈出的又一个重要步伐。他们太久以来一直承受着难以想象的诊断之旅的重负,被告知除了支持性治疗之外没有其他治疗方法,然后不得不看着自己的孩子消逝,”Orchard Therapeutics联合创始人兼首席执行官Bobby... 查看详情
22
9月
FDA接受TAK-721(布地奈德口服混悬剂)用于嗜酸性粒细胞性食管炎短期治疗的重新申请
武田制药宣布,美国食品和药物管理局(FDA)已接受其新药申请(NDA)的再次提交,该申请用于研究短期治疗嗜酸性食管炎(EoE)的TAK-721(布地奈德口服悬浊液),这是一种慢性炎症性疾病,可以损害食管。 此次重新提交旨在解决FDA对公司原始NDA提交的反馈。 武田肝胆胃肠病美国医学部门负责人、医学博士Vijay Yajnik博士表示:“武田对TAK-721的关注源于我们的信念,嗜酸性食管炎社区存在重大未满足的治疗需求。” “在过去的几个月里,我们重新分析了TAK-721的临床数据,并与FDA展开了对话,因为我们认识到EoE患者需要更多的治疗选择。 由于这次富有建设性的讨论,我们已经重新提交了... 查看详情
22
9月
美国FDA批准NXC-201用于治疗淀粉样蛋白轻链(AL)淀粉样变性的孤儿药认定
Immix Biopharma生物制药公司宣布,美国食品和药物管理局(FDA)已批准NXC-201用于治疗一种危及生命的血液疾病——轻链淀粉样(AL)淀粉样病的孤儿药物认定(ODD)。NXC-201是一种下一代CAR-T细胞疗法,目前正在进行1b/2a临床试验NEXICART-1(NCT04720313)的评估。 FDA的孤儿产品开发办公室将孤儿认定状态授予旨在安全有效治疗、诊断或预防罕见疾病或在美国影响少于20万人的药物和生物制品。孤儿药物认定提供了一些福利,包括财政激励,以支持临床开发,并在获得监管批准后在美国获得长达7年的市场排他性。 三大好消息: “我们很高兴为NXC-201在AL淀粉... 查看详情
21
9月
欧盟委员会批准Orserdu(elacestrant)用于ESR1突变/ER阳性/HER2阴性乳腺癌
乳腺癌是女性中常见的一种癌症,也影响着一些男性。而在乳腺癌的治疗中,激素受体阳性(ER+)乳腺癌占有一席之地,因此寻找有效的治疗方法一直是医学界的焦点。近期,欧洲委员会(European Commission)批准了一种新的药物——Elacestrant(商品名:Orserdu),用于治疗激素受体阳性(ER+)、人表皮生长因子受体2阴性(HER2–)的乳腺癌患者,特别是那些具有活化的ESR1突变并在至少接受过一线内分泌治疗(包括CDK4/6抑制剂)后疾病进展的乳腺癌患者。 Orserdu(elacestrant)的获批 Orserdu(elacestrant)的获批是基于来自EMERALD试验... 查看详情
21
9月
欧盟批准Litfulo(利特昔替尼)治疗12岁以上重度斑秃
斑秃是一种影响数百万人的自体免疫性疾病,它让患者失去了头发,不仅影响了外貌,还可能对患者的自尊心和生活质量造成重大影响。然而,好消息是,医学界不断努力寻找有效的治疗方法。在这篇文章中,我们将介绍辉瑞公司的JAK3抑制剂利特昔替尼(Litfulo)的获批情况,以及它如何改善12岁以上重度斑秃患者的生活。 革命性的斑秃治疗方案 辉瑞公司在2023年9月19日宣布,欧盟委员会已批准其JAK3抑制剂利特昔替尼(Ritlecitinib)胶囊用于治疗12岁及以上青少年和成人重度斑秃。这一获批上市的决定基于一项名为ALLEGRO的随机、双盲、安慰剂对照的IIb/III期研究,该研究的目标是评估Ritlec... 查看详情
21
9月
HIV预防Apretude(cabotegravir)长效方案获欧盟授权
HIV感染仍然是全球健康领域的一大挑战,尤其是对于高危人群。然而,最新的医疗进展为HIV预防带来了新的曙光。 革命性的HIV预防方案 ViiV Healthcare在9月19日宣布,欧盟委员会已正式授权Apretude(cabotegravir长效注射剂和片剂)用于预防HIV感染。Cabotegravir是一种适用于高危成年人和青少年(至少12岁)的HIV预防方案,适用于与暴露前预防(PrEP)的安全性行为结合使用,以降低他们的性获得性HIV-1感染风险。最引人注目的特点之一是,Cabotegravir长效注射剂和片剂成为欧盟批准的第一个、也是唯一一个将HIV预防所需的剂量从每日服药减少到每年... 查看详情
21
9月
FDA将优先审查肾细胞癌靶向疗法Welireg(belzutifan)的补充新药
肾细胞癌(RCC)作为肾癌的最常见形式,一直是医学界和患者面临的重大挑战之一。肾细胞癌通常在不经意的情况下被发现,对患者的生活质量和生存构成了威胁。然而,令人振奋的消息是,药物Welireg(belzutifan)可能为晚期肾细胞癌患者带来新的希望。美国食品药品监督管理局(FDA)已同意对Welireg(belzutifan)的补充新药申请进行优先审查,这标志着一项潜在的肾细胞癌靶向疗法即将问世。 肾细胞癌的严峻挑战 肾细胞癌是肾癌中的主要类型,约占肾癌病例的九成。这一癌症在男性中的发病率是女性的两倍,使其成为男性罹患的高发癌症之一。令人不安的是,大多数肾细胞癌病例都是在进行其他腹部疾病的影像... 查看详情
20
9月
Tislelizumab(Tevimbra)在欧洲获批用于铂类化疗后的晚期食管鳞癌
食管鳞癌(ESCC)是一种恶性肿瘤,常常在诊断时已经进展到晚期,对治疗造成了巨大挑战。然而,一项新的生物制剂已获得欧洲委员会批准,为晚期ESCC患者带来了新的希望。该生物制剂名为Tislelizumab(Tevimbra),它被批准用于接受过铂类化疗的成年患者,这些患者患有不可切除的、局部晚期或转移性食管鳞癌。 改善患者生存期 Tislelizumab的批准基于RATIONALE 302试验的数据,该试验表明,在意图治疗(ITT)人群中,接受Tislelizumab治疗的患者在总生存期(OS)方面表现出明显的统计学和临床意义上的改善,与接受医生选择的化疗治疗的患者相比(HR,0.70;95% ... 查看详情
20
9月
Tislelizumab(Tevimbra)一线治疗食管鳞癌申请FDA批准
食管鳞癌(食道鳞状细胞癌,ESCC)是一种具有挑战性的癌症类型,通常在晚期才被发现,难以治疗。然而,一项新的生物制药申请已提交FDA审批,旨在改善这一情况。该申请寻求批准使用Tislelizumab(Tevimbra)作为一线治疗,用于治疗不可切除、复发、局部晚期或转移性食管鳞癌患者。 一项潜在的重要突破 Tislelizumab是一种PD-1抗体,已在某些其他类型的癌症治疗中取得了显著的突破。现在,它有望成为食管鳞癌治疗的一部分。 这一申请得到了来自RATIONALE 306(NCT03783442)研究的支持,该研究发现,将Tislelizumab与化疗联合使用可以改善患者的总生存期(OS... 查看详情
20
9月
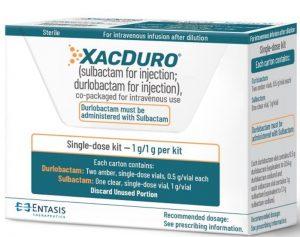
不动杆菌终有克星!Xacduro(舒巴坦,杜洛巴坦)打破不动杆菌耐药性的抗生素突破
抗生素是现代医学中不可或缺的工具,但随着时间的推移,细菌的耐药性逐渐崭露头角,成为医学界面临的一大挑战。在这个背景下,针对一种致命细菌——不动杆菌(也称为鲍氏不动杆菌)的耐药性感染,常常让医生束手无策。然而,一项重要的突破已经出现在医学领域:Xacduro(注射用舒巴坦;注射用杜洛巴坦),这是首个专门针对不动杆菌的抗生素,已获得美国FDA批准,用于治疗医院获得性细菌性肺炎(HABP)和呼吸机相关性细菌性肺炎(VABP)的成年患者。 不动杆菌的威胁 不动杆菌是一种革兰氏阴性菌,通常在医疗机构中引起感染,其中以肺炎最为常见。然而,不动杆菌感染如今已经成为全球第五大由耐药性引起的最常见死因,对于使用... 查看详情