19
8月
FDA批准Veopoz(pozelimab-bbfg)作为首个治疗儿童和成人CHAPLE的药物
再生元制药公司今天宣布,美国食品和药物管理局(FDA)已批准Veopoz™(pozelimab-bbfg)用于治疗1岁及以上的成人和儿科CHAPLE患者,也称为CD55缺陷蛋白丢失性肠病。Veopoz是首个也是唯一一个专门用于治疗CHAPLE的药物。随着Veopoz的批准,与afliberept 8mg BLA相关的预批准检查问题已经得到解决。FDA预计将在未来几周内对afliberept 8 mg BLA采取行动。 “大多数CHAPLE患者是儿童,他们在婴儿期就面临严重的衰弱症状和经常危及生命的并发症,”免疫系统部门分子发育主任Michael Lenardo医学博士说;美国国立卫生研究院(N... 查看详情
18
8月
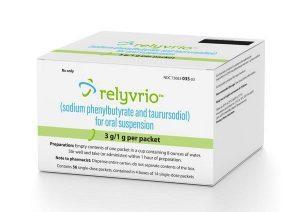
肌萎缩侧索硬化新药Relyvrio的服用方法及使用须知
肌萎缩侧索硬化(ALS)是一种难以治疗的进行性神经退行性疾病,给患者的生活带来了巨大挑战。尽管目前还没有可以完全治愈ALS的方法,但近期获得FDA批准的药物Relyvrio(苯丁酸钠和牛磺酸二醇)为患者带来了新的希望。本文将介绍如何正确服用Relyvrio,以及患者可能会遇到的问题和解决方法。 ALS:挑战与希望 ALS是一种神经系统疾病,其特点是神经细胞逐渐退化,导致肌肉萎缩和运动功能丧失。尽管目前仍然没有彻底治愈的方法,但科学家和医生们一直在努力寻找能够减缓疾病进展的方法。Relyvrio的批准为ALS患者带来了新的曙光,或许能够帮助他们更好地应对这一复杂的疾病。 剂量建议:逐步增加 Re... 查看详情
18
8月
抗肥胖药物利拉鲁肽(Liraglutide)改善肥胖者的联想学习
研究人员报告说,由肥胖引起的联想学习障碍可以通过利拉鲁肽(Liraglutide)(一种抗肥胖药物)来恢复。 研究人员表示,与一组不肥胖的参与者相比,只服用了一剂后,肥胖的研究参与者没有出现任何损害。 他们说,这意味着这种药物不仅可以通过刺激胰岛素分泌来治疗肥胖,还可以通过促进联想学习来帮助治疗肥胖,从而提高动力。 新的研究表明,旨在控制肥胖的干预措施也具有提高大脑学习能力的额外效果——只需一次剂量。 这项工作是由德国科隆马克斯普朗克代谢研究所的研究人员进行的,并得到了科隆大学和科隆大学医院的资助。 研究结果发表在今天的《自然代谢》杂志上。 马克斯·普朗克研究所(Max Planck Inst... 查看详情
18
8月
AOC 1044获孤儿药资格用于治疗DMD44突变杜氏肌营养不良症
科技的不断进步带来了医学领域的革命性突破。近日,Avidity生物科学公司欣喜宣布,其创新药物AOC 1044已获得美国食品和药物管理局(FDA)的孤儿药资格,将用于治疗可外显子44跳变(DMD44)突变引起的杜氏肌营养不良症。这一重大突破为罕见疾病的治疗带来了新的曙光。 孤儿药资格的重要里程碑 在医学研究领域,罕见疾病往往受到医疗界的关注不足。然而,正是这些疾病才是许多患者生活中的沉重负担。Avidity生物科学公司的AOC 1044药物获得孤儿药资格,意味着针对DMD44突变引起的杜氏肌营养不良症的治疗进入了新的阶段。在此之前,外显子44的疗法一直是一个未被突破的难题,AOC 1044的获... 查看详情
18
8月
治疗抗精神病药物引起的体重增加的1B期临床试验成功完成
Response Pharmaceuticals, Inc.今天宣布,该公司的主要候选药物RDX-002成功完成了1B期临床试验,RDX-002是一种肠道微粒体甘油三酯转移蛋白(iMTP)的一流抑制剂。在对全部结果进行分析时,RDX-002总体耐受性良好,该研究达到了其主要目标。该公司正与其科学团队和顾问委员会合作,完成数据分析并准备最终的完整结果。 Response Pharmaceuticals的1B期试验是一项为期2周的开放标签研究,参与者为antipsychotic-naïve健康志愿者。所有受试者最初使用奥氮平治疗一周,奥氮平是一种广泛使用的抗精神病药物,其副作用是体重增加,然后一组... 查看详情
18
8月
FDA批准Sohonos (palovarotene)用于治疗进行性骨化性纤维发育不良
法国巴黎,2023年8月16日-易普森(Euronext: IPN;美国食品和药物管理局(FDA)今天宣布,Sohonos™(palovarotene)胶囊被批准作为类维生素a,用于减少8岁及以上女性和10岁及以上男性进行性骨化纤维发育不良(FOP)成人和儿科患者的新异位骨化体积。 “FDA批准Sohonos是美国FOP界的一个突破。这是医生第一次拥有一种经批准的药物,可以减少新的、异常骨骼生长的形成,即异位骨化(HO),异位骨化会导致使人衰弱的行动能力挑战,并对FOP患者的生活产生破坏性影响,”易普森公司研发主管Howard Mayer说。“罕见病药物的开发需要每个参与者的承诺和信念。我们在... 查看详情
17
8月
基因工程纳米囊泡:更有效地靶向癌细胞
在化疗方面存在两个令人遗憾的事实:它不仅会伤害癌细胞,也会伤害健康细胞,而且许多治疗靶点都位于癌细胞内部,使得治疗变得更加困难。 纽约州立大学宾汉姆顿分校的生物医学工程师们正在研究使用细胞来源的纳米囊泡将治疗剂传递到癌细胞内部,以更准确、更高效地进行治疗。细胞释放的一种蛋白质、脂质和RNA组成的小囊泡被称为纳米囊泡,它们用作细胞间通讯的方法,可以被改造用于携带药物。 纳米囊泡:治疗靶向的有力工具 宾汉姆顿分校托马斯·J·沃森工程与应用科学学院生物医学工程系助理教授袁婉表示:“这些纳米载体具有一些优异的特性。例如,它们可以从人类细胞株中获取,因此免疫反应非常低。这可以实现最佳生物相容性,使其逃避... 查看详情
17
8月
儿童不可治愈脑肿瘤的生存率提高:裂缝中的突破
医学领域的不断发展带来了许多希望,其中一个值得关注的突破是,在缺乏有效治疗方法的情况下,研究人员找到了一种潜在的药物候选物,能够改善一种儿童脑肿瘤患者的预后。这种名为ONC201的化合物使得患有弥漫性中线胶质瘤(DMG)或弥漫性内源性桥脑胶质瘤(DIPG)的患者的生存率几乎翻倍,与之前的患者相比。 研究发现:为无药可治的脑肿瘤提供新希望 这一发现是由密歇根大学健康罗杰肿瘤中心和查德·卡尔儿童脑肿瘤中心的国际研究团队报告的。除了对两个早期临床试验结果的报告外,这篇论文还揭示了这种化合物在这些肿瘤中成功的潜在机制。该论文发表在《癌症发现》杂志上,这是美国癌症研究协会的一份刊物。 弥漫性中线胶质瘤,... 查看详情
17
8月
美国儿科学会建议给所有婴儿提供预防呼吸道合胞病毒的药物
Nirsevimab是一种长效单克隆抗体,可以挽救生命,防止成千上万的婴儿因严重疾病住院。 ITASCA, IL——美国儿科学会建议所有婴儿,尤其是高危婴儿,接受新的预防抗体nirsevimab,以预防由呼吸道合胞病毒(RSV)引起的严重疾病,RSV是一种常见的、高度传染性的,有时是致命的疾病。 Nirsevimab是一种长效单克隆抗体,通过注射给药。这种抗体增强了免疫系统,为抵御呼吸道合胞病毒引起的严重疾病增加了一层额外的防御。AAP强调了公平获得nirseimab的必要性,同时承认,与任何新产品一样,它不会立即在所有临床环境中可用。美国儿科学会还建议,在2023-2024 RSV流行季期间... 查看详情
16
8月
Tecentriq(atezolizumab阿特珠单抗)显著提高不适合铂类化疗的NSCLC患者总生存率
近期,《柳叶刀》杂志在线发表的一项研究揭示了非小细胞肺癌(NSCLC)领域的一项重要发现:一线使用Tecentriq(atezolizumab阿特珠单抗)单药治疗在一类特定患者中显示出了显著的生存优势。这一成果有望为肺癌患者提供新的治疗希望,值得我们深入探讨。 新的治疗方向:atezolizumab单药治疗NSCLC 伦敦大学学院的Siow Ming Lee医学博士及其团队开展了一项跨国研究,共涉及23个国家的91个研究地点,该研究的结果表明,对于不适合铂类化疗的NSCLC患者,一线使用atezolizumab单药治疗相较于传统的单一药物化疗,显著提高了总生存率。在这项涵盖453名患者的随机对... 查看详情