22
6月
TEVA梯瓦公司推出新的“转向增长”战略
以色列特拉维夫–(美国商业资讯)–梯瓦制药工业有限公司(纽约证券交易所和特拉维夫证券交易所代码:TEVA)今天宣布了一项新的战略框架,该框架包含四大支柱,旨在使公司进入新的增长时代。该战略旨在通过 AUSTEDO ®、 AJOVY ®、UZEDY和生物仿制药扩大了其创新产品线,维持其仿制药实力并专注于业务。这四大支柱预计将为患者带来更高的价值并产生更大的影响。 Teva 总裁兼首席执行官 Richard Francis表示:“我们的新战略建立在四个关键支柱之上,通过我们的商业产品组合和生物仿制药、创新管道、仿制药巨头和集中的资本配置实现短期和长期增长。 ” “通过我们的... 查看详情
22
6月
MedinCell:mdc-TJK(Teva 的代号:TEV-44749)1 期研究药代动力学由 Teva 在 SIRS 2023 上首次展示
MedinCell 的合作伙伴 Teva Pharmaceuticals在 2023 年精神分裂症研究协会 (SIRS) 上发表一份原始报告,描述奥氮平长效皮下制剂(mdc-TJK 或 TEV-44749)的药代动力学特征。 将提供的数据来自一项 127 名参与者的 1 期临床研究,该研究评估了单次递增剂量 mdc-TJK (TEV-44749) 在健康志愿者中的药代动力学,以及在精神分裂症患者中每月一次和多次剂量的药代动力学或分裂情感障碍。注射后,mdc-TJK (TEV-44749) 在一天内达到治疗浓度,并在整个 28 天的给药间隔内维持该浓度。 mdc-TJK (TEV-44749) ... 查看详情
21
6月
Teva 和 MedinCell 的合作關係
关于精神分裂症 精神分裂症是一种慢性、进行性和严重使人衰弱的精神障碍,影响一个人的思维、感觉和行为。患者会出现一系列症状,其中可能包括妄想、幻觉、言语或行为紊乱以及认知能力受损。世界上大约 1% 的人口会在其一生中患上精神分裂症,目前在美国有 350 万人被诊断出患有这种疾病。尽管精神分裂症可以发生在任何年龄,但男性的平均发病年龄往往在十几岁到 20 岁出头,而女性则在 20 多岁到 30 岁出头。精神分裂症的长期病程以部分或完全缓解被复发打破为特征,这通常发生在精神科急症的情况下,需要住院治疗。大约 80% 的患者在治疗的前五年经历了多次复发,每次复发都会带来功能丧失、治疗难治和脑形态改变的... 查看详情
21
6月
Teva 和 MedinCell 宣布 FDA 批准 UZEDY™(利培酮)缓释注射混悬液,一种长效皮下非典型抗精神病注射液,用于 治疗成人精神分裂症
新泽西州帕西帕尼、特拉维夫和巴黎,2023 年 4 月 28 日– Teva Pharmaceutical Industries Ltd.(纽约证券交易所和 TASE:TEVA)的美国子公司 Teva Pharmaceuticals 和 MedinCell(泛欧交易所代码:MEDCL)今天宣布,美国食品和药物管理局(FDA) 已批准 UZEDY(利培酮)缓释可注射混悬液用于治疗成人精神分裂症。UZEDY 是利培酮的第一个皮下长效制剂,它利用 SteadyTeq™,MedinCell 专有的一种共聚物技术,可控制利培酮的稳定释放。单次给药后 6-24 小时内可达到治疗血药浓度。 “UZEDY 体... 查看详情
20
6月
Genentech 提供了新数据,证明 Glofitamab 和 Mosunetuzumab 作为固定期限、现成的淋巴瘤治疗方案的潜力
在 2022 年 12 月 10 日至 13 日举行的第 64 届美国血液学会 (ASH) 年会和博览会上进行了介绍。研究性双特异性 glofitamab 在复发或难治性 (R/R) 大 B-细胞淋巴瘤 (LBCL) 表明 glofitamab 有可能成为第一个现成的 CD20xCD3 T 细胞结合双特异性抗体,可以在固定的时间内给予患有严重预处理的侵袭性淋巴瘤的人。这些数据将在会上呈现,并同步在线发布于新英格兰医学杂志 (NEJM)。此外,mosunetuzumab 的更新数据继续证明在经过大量预处理的滤泡性淋巴瘤 (FL) 患者中具有临床意义的结果。Mosunetuzumab 是一种固定疗... 查看详情
20
6月
FDA 批准基因泰克(Genentech)的 Columvi,这是第一个也是唯一一个对复发或难治性弥漫性大 B 细胞淋巴瘤患者进行固定疗程治疗的双特异性抗体
加利福尼亚州南旧金山–( BUSINESS WIRE )–(美国商业信息)–罗氏集团 (6: RO, ROG; OTCQX: RHHBY) 的成员基因泰克 (Genentech) 今天宣布,美国食品和药物管理局 (FDA) 已批准 Columvi ®(glofitamab-gxbm) 用于治疗复发或难治性 (R/R) 未另行说明的弥漫性大 B 细胞淋巴瘤 (DLBCL) 或由滤泡性淋巴瘤引起的大 B 细胞淋巴瘤 (LBCL) 的成年患者,经过两次或两次以上治疗系统治疗线。该适应症根据 I/II 期 NP30179 研究中的反应率和反应持久性获得加速批准。对该... 查看详情
20
6月
全球双特异性抗体市场机会和临床试验洞察 2023 报告
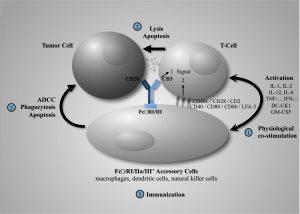
基于抗体的疗法的引入已经改变了癌症治疗领域的游戏规则。单克隆抗体已经存在了几十年,并且仍然发挥着如此重要的作用。然而,随着临床上未满足的医疗需求不断增加,目前的工作重点是开发这些生物制剂的先进形式。抗体生物制品研发的持续扩张带来了双特异性抗体时代。 这些双特异性抗体能够参与或靶向两个不同的目标,因此能够同时执行多种操作,包括:将免疫细胞引导至肿瘤细胞,同时阻断两种不同的途径并传递细胞毒性有效载荷。在过去的几十年里,双特异性抗体的生产遇到了很多困难;尽管如此,它们已显示出作为有前途的癌症疗法的巨大潜力。 双特异性抗体是一种快速发展的工程生物制品,显著改善了未满足的重大医疗需求。Columvi 的... 查看详情
20
6月
罗氏与艾伯维在新的双特异性抗体(bispecific antibody, BsAb) 淋巴瘤市场份额的竞争
在竞争对手 AbbVie 的淋巴瘤双特异性抗体获批 4 周后, FDA 周四批准罗氏集团成员 Genentech 的 BsAb 用于复发或难治性弥漫性大 B 细胞淋巴瘤。 两家公司的双特异性抗体将于今年夏天上市,一场正面交锋正在酝酿之中。 Genentech 的 Columvi (glofitamab) 和 AbbVie 的 Epkinly (epcoritamab) 已上市,用于治疗复发或难治性弥漫性大 B 细胞淋巴瘤 (DLBCL),这是最常见的非霍奇金淋巴瘤类型。Columvi 还被批准用于治疗由滤泡性淋巴瘤引起的大 B 细胞淋巴瘤 (LBCL)。同时,Epkinly也适用于因惰性淋巴瘤... 查看详情
20
6月
COLUMVI(注射用 Glofitamab)获得加拿大卫生部批准,有条件用于成人复发或难治性弥漫性大 B 细胞淋巴瘤患者
安大略省密西沙加市——2023 年 3 月 25 日——霍夫曼罗氏有限公司(罗氏加拿大)今天宣布,加拿大卫生部于 2023 年 3 月 24 日批准 COLUMVI(注射用 glofitamab)用于治疗复发或难治性弥漫性大 B 细胞成年患者未另行说明的淋巴瘤 (DLBCL)、滤泡性淋巴瘤 (trFL) 引起的 DLBCL 或原发性纵隔 B 细胞淋巴瘤 (PMBCL),已接受两线或更多线的全身治疗且不符合或不能接受 CAR-T 细胞疗法或之前接受过 CAR-T 细胞疗法。[4] COLUMVI已获得有条件的上市许可,等待试验结果验证其临床益处。 大 B 细胞淋巴瘤包括影响淋巴系统 B 细胞的... 查看详情
20
6月
罗氏格罗菲妥单抗(Glofitamab)注射液中国申报上市
2023年2月1日,中国国家药监局药品审评中心(CDE)官网公示,由罗氏(Roche)开发的格罗菲妥单抗(Glofitamab)注射液在中国提交的上市申请(BLA)获得中国药监局审评中心(NMPA)受理。Glofitamab的适应症为治疗既往接受过至少两线系统性治疗的复发或难治性弥漫大B细胞淋巴瘤(Relapsed or Refractory Large B-cell Lymphoma, DLBCL)和原发性纵隔大B细胞淋巴瘤(Primary Mediastinal Large B-cell Lymphoma, PMBL)成人患者。上个月,Glofitamab刚获得用于三线及以上治疗复发或难治... 查看详情