24
10月
Orgovyx(Relugolix)治疗晚期前列腺癌在加拿大获批
2023年10月23日,加拿大卫生部宣布批准ORGOVYX®(relugolix),一种口服促性腺激素释放激素(GnRH)受体拮抗剂,用于治疗晚期前列腺癌。这一批准标志着加拿大迎来了一项重大医学突破,将为晚期前列腺癌患者提供一种创新治疗选择。 ORGOVYX:突破性前列腺癌治疗药物 前列腺癌是加拿大男性最常见的癌症之一,每年数以万计的男性受到其影响。在晚期前列腺癌的治疗方面,雄激素剥夺疗法一直是主要的治疗手段。这种疗法旨在将睾酮水平降低到极低水平,通常被称为去势水平,以抑制前列腺癌的生长。然而,传统的治疗方法可能伴随着一些限制和不良反应,包括睾酮水平的初始激增和治疗停药后的恢复延迟。ORGOV... 查看详情
24
10月
FDA批准Cabtreo(克林霉素/阿达帕林/过氧化苯甲酰)外用凝胶治疗寻常型痤疮
2023年10月20日,美国食品和药物管理局(FDA)正式批准了一项里程碑性的皮肤科治疗药物,CABTREO(克林霉素/阿达帕林/过氧化苯甲酰)外用凝胶。这一批准将使得12岁及以上的寻常型痤疮患者可以获得更有效的局部治疗。CABTREO是迄今为止唯一一种获得FDA批准的三联组合痤疮治疗药物,将为痤疮患者带来新的希望。本文将详细介绍CABTREO的特点,临床试验结果以及对痤疮患者的积极影响。 CABTREO:一项突破性的痤疮治疗药物 寻常型痤疮,即面部痤疮,是美国最常见的皮肤问题之一,影响着数千万美国人。这种常见皮肤问题的形成是由于毛囊被皮脂和皮肤细胞阻塞,进而导致面部、前额、胸部、上背部和肩膀... 查看详情
23
10月
FDA批准Penbraya(五价脑膜炎球菌疫苗)用于预防青少年脑膜炎球菌病最常见血清型
2023年10月20日,辉瑞公司(Pfizer)宣布美国FDA已正式批准Penbraya(五价脑膜炎球菌疫苗),这款疫苗将为10至25岁的青少年和年轻人提供强有力的保护,预防了脑膜炎球菌病最常见血清型的侵袭性感染。这一消息在医学界引起了广泛的关注和期待。 Penbraya:预防脑膜炎球菌病的新希望 Penbraya疫苗(meningococcal groups A, B, C, W and Y vaccine)标志着预防脑膜炎球菌病迈出的重要一步。这是一种包含了五种脑膜炎球菌血清型的疫苗,它针对A、B、C、W和Y血清型的侵袭性脑膜炎球菌疾病提供了全面的保护。此前,针对不同血清型的脑膜炎球菌疫苗... 查看详情
22
10月
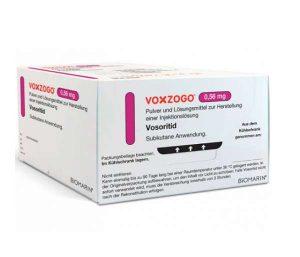
FDA批准VOXZOGO(Vosoritide,伏索利肽)治疗5岁以下软骨发育不全儿童
2023年10月20日,BioMarin Pharmaceutical Inc.宣布美国食品和药物管理局(FDA)已批准VOXZOGO®(vosoritide,伏索利肽)的补充新药申请(sNDA),以拓展其适应症范围,治疗软骨发育不全儿童。这一重要的批准标志着医学领域的一项突破性成就,将为5岁以下的儿童带来更好的生长和生活质量。 伏索利肽VOXZOGO的扩大适应症 VOXZOGO之前适用于5岁及以上的儿童,但最新的批准已将其适应症范围扩展至包括所有年龄段的儿童,具有开放生长板的软骨发育不全患者。这一决策是基于VOXZOGO在随机、双盲、安慰剂对照的2期临床试验中所展现出的卓越安全性和有效性。不... 查看详情
21
10月
FDA批准Maxigesic(扑热息痛/布洛芬)注射剂治疗术后中度至重度疼痛
手术后疼痛是许多患者面临的常见问题,而阿片类药物的滥用却引发了一场全球性的卫生危机。然而,随着新药的研发和批准,疼痛管理领域正发生积极的变革。于2023年10月18日,比利时列日的Hyloris Pharmaceuticals SA生物制药公司宣布,其Maxigesic® IV药物已经获得美国批准,用于缓解成人轻度至中度疼痛以及治疗中度至重度疼痛,成为成人阿片类镇痛药的辅助药物。这一重要的药物批准不仅带来了新的疼痛管理选择,还为手术后疼痛管理领域注入了新的活力。 Maxigesic® IV的突破性 新药申请 (NDA) 的批准源于一个经过充分研究和试验的计划,其中Maxigesic® IV展现... 查看详情
20
10月
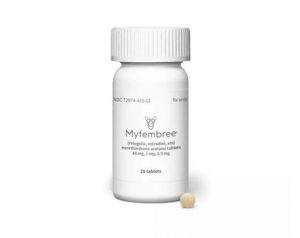
加拿大批准Myfembree(Relugolix复方片)治疗子宫内膜异位症及子宫肌瘤
最近,住友制药加拿大公司和辉瑞加拿大公司宣布,加拿大卫生部已批准Myfembree(Relugolix、雌二醇和醋酸炔诺酮)用于治疗绝经前妇女与子宫内膜异位症相关的中度至重度疼痛。这是一项重要的决定,为那些饱受这些疾病之苦的患者提供了新的治疗选择。Myfembree已经在美国获得批准,现在在加拿大也可用,这将有望改善许多女性的生活质量。 Myfembree的双重适应症批准 Myfembree是一种联合疗法,包含雌激素和醋酸炔诺酮。此药已获得双重适应症批准,成为加拿大卫生部批准的第一个治疗子宫内膜异位症和子宫肌瘤的口服治疗药物。其首次批准用于治疗与子宫肌瘤相关的大量月经出血,随后又批准用于治疗与... 查看详情
20
10月
FDA授予ANPD001治疗帕金森病的快速通道地位
2023年10月19日,美国圣地亚哥(San Diego),Aspen Neuroscience高兴地宣布,美国食品药物管理局(FDA)已授予ANPD001快速通道地位,用于改善帕金森病(PD)患者的运动功能。这一消息为医学界和PD患者带来了新的希望,因为ANPD001是一种正在研究中的个性化(自体)细胞疗法,旨在通过替代丧失的多巴胺神经元来治疗PD。 快速通道地位的意义 快速通道地位的目的是尽早将重要的新药物推向患者。FDA授予快速通道地位(FTD)旨在促进药物的开发,并加速审批治疗严重疾病并填补未满足医疗需求的药物。快速通道地位的好处包括在临床开发过程中与FDA的早期和频繁互动,以及获得加... 查看详情
19
10月
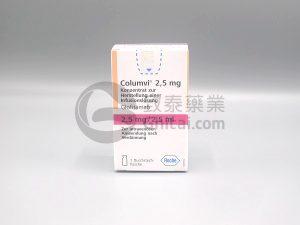
Columvi(glofitamab)用于治疗晚期淋巴瘤获美国NICE推荐
淋巴瘤是一组与淋巴系统相关的癌症,其中弥漫性大B细胞淋巴瘤(DLBCL)是最常见的亚型之一。每年,数千名英国居民被诊断患有DLBCL,这一罕见疾病的典型症状包括无痛性肿胀、盗汗、发烧和体重减轻。当前,未经治疗的DLBCL通常使用R-CHOP疗法,但该治疗仅对50-70%的患者有效。然而,最近的突破性药物,Columvi(glofitamab),为DLBCL患者带来了新的希望,该药已被美国国家健康和护理卓越研究所(NICE)推荐作为新的治疗选择。 DLBCL:一种挑战性的癌症 弥漫性大B细胞淋巴瘤是一种罕见而复杂的癌症。它可以在任何年龄发生,但多数患者在65岁或更老时才被诊断出。其症状可能不明显... 查看详情
19
10月
ADCETRIS(维布妥昔单抗)联合AVD获欧盟批准治疗霍奇金淋巴瘤
2023年10月18日,武田(Takeda)宣布欧盟委员会(EC)已批准ADCETRIS®(维布妥昔单抗,brentuximab vedotin)与阿霉素、长春花碱和达卡巴嗪(AVD)联合使用,用于治疗既往未经治疗的CD30+III期霍奇金淋巴瘤成年患者。 霍奇金淋巴瘤是一种恶性淋巴系统疾病,而CD30是其特定标志物。ADCETRIS®是一种靶向CD30的抗体药物偶联物(ADC),通过释放微管破坏剂单甲基auristatin E(MMAE)来对抗肿瘤细胞,利用Seagen的专有技术,这一突破性疗法将为患者带来新希望。 一、前所未有的治疗选择: 在此之前,ADCETRIS®已经被批准用于治疗欧洲... 查看详情
19
10月
FDA批准Bimzelx(bimekizumab-bkzx)治疗中度至重度银屑病
2023年10月18日,全球生物制药公司UCB宣布,美国食品和药物管理局(FDA)已批准Bimzelx(bimekizumab-bkzx)用于治疗中度至重度银屑病的成年患者,这些患者适合接受系统治疗或光疗。Bimekizumab是首个并且唯一批准用于选择性抑制两种主要细胞因子——白细胞介素17A(IL-17A)和白细胞介素17F(IL-17F)的治疗银屑病药物。Bimekizumab的批准得到了三个阶段3、多中心、随机对照试验(BE READY、BE VIVID和BE SURE)的数据支持,这些试验评估了1480名中度至重度银屑病成年患者的疗效和安全性。 一、创新的里程碑: UCB美国免疫解决... 查看详情