23
7月
Uzpruvo治疗克罗恩病、银屑病关节炎和斑块状银屑病在欧盟获批
欧洲推出的突破性药物 近日,德国巴特菲尔贝尔和冰岛雷克雅未克的制药公司STADA和Alvotech宣布,在大多数欧洲国家成功推出了名为Uzpruvo®的生物仿制药。这款药物是欧洲首个获批的Stelara®(Ustekinumab)生物仿制药,标志着生物仿制药市场的重要里程碑。 Uzpruvo的批准与适应症 今年1月,Uzpruvo成功获得欧盟委员会的批准,成为首个乌司他单抗的生物仿制药。Uzpruvo在疗效、安全性、药代动力学和免疫原性方面与Stelara®参考产品相当。其适应症包括成人克罗恩病和银屑病关节炎,以及成人和6岁以上儿童的斑块状银屑病。然而,由于原研公司仍拥有溃疡性结肠炎适应症的独... 查看详情
21
7月
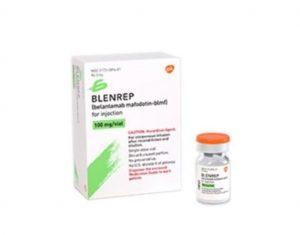
EMA接受Blenrep(belantamab mafodotin)组合治疗复发/难治性多发性骨髓瘤的上市许可申请
近期,欧洲药品管理局(EMA)正式接受了关于belantamab mafodotin(商品名:Blenrep)联合bortezomib(商品名:Velcade)和地塞米松(BVd),或联合泊马度胺(商品名:Pomalyst)和地塞米松(BPd)治疗复发或难治性多发性骨髓瘤患者的上市授权申请。这一申请基于DREAMM-7和DREAMM-8两项III期临床试验的中期数据,这两项试验均显示,belantamab mafodotin组合方案在无进展生存期(PFS)方面较标准治疗方案(SOC)有显著改善。 DREAMM-7和DREAMM-8试验的初步成果 在DREAMM-7试验中,接受BVd治疗的患者(... 查看详情
21
7月
vimseltinib用于治疗腱鞘巨细胞瘤获欧盟药品管理局受理
近日,欧洲药品管理局(EMA)正式受理了一项关于靶向药物vimseltinib的市场授权申请(MAA),该药物被提议用于治疗腱鞘巨细胞瘤(TGCT)患者。这一进展意味着vimseltinib有望成为这种罕见病的新疗法,给众多需要有效且耐受性良好治疗的 TGCT 患者带来希望。 关键临床试验 MOTION 的积极结果 这一市场授权申请是基于一项名为 MOTION 的三期临床试验(NCT05059262)的结果。该试验是一项国际性、随机、双盲、安慰剂对照的研究,共纳入了83名确诊为有症状 TGCT 的患者,另有40名患者接受安慰剂治疗。研究结果显示,在第25周时,vimseltinib治疗组的客观... 查看详情
19
7月
FDA授予树突状细胞疫苗DOC1021治疗胰腺癌的快速通道地位
美国食品药品监督管理局(FDA)已经批准Diakonos Oncology公司开发的树突状细胞疫苗(DCV)DOC1021,用于胰腺导管腺癌(PDAC)患者的快速通道资格。此次批准基于该疫苗在I期临床试验中展现出的良好疗效,尤其是对于胶质母细胞瘤(GBM)患者的显著生存期延长。 DOC1021疫苗在胶质母细胞瘤中的初步成功 在2024年美国癌症研究协会年会上,研究人员展示了DOC1021疫苗在I期临床试验中的成果。数据显示,受试的胶质母细胞瘤患者中位总生存期尚未达到,12个月生存率高达88%,这与传统治疗方法相比是一个显著的提升。在16名可评估的GBM患者中,有12名仍然存活,并且没有出现严重... 查看详情
19
7月
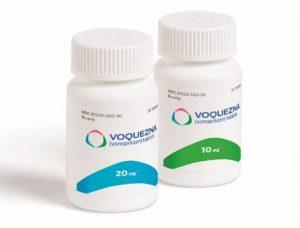
VOQUEZNA(Vonoprazan,沃诺拉赞)用于非糜烂性胃食管反流病治疗获FDA批准
2024年7月18日,Phathom Pharmaceuticals, Inc.公司宣布,美国食品药品管理局(FDA)已正式批准VOQUEZNA®(vonoprazan,沃诺拉赞)10mg片剂用于缓解成人非糜烂性胃食管反流病(Non-Erosive GERD)相关的胃灼热症状。这一重要决定为广大患者提供了一种全新的治疗选择,并为非糜烂性GERD的药物治疗开辟了新的篇章。 关键研究:PHALCON-NERD-301的成功 VOQUEZNA®获得批准的背后,是PHALCON-NERD-301研究的强力支撑。这项研究是一项3期随机、安慰剂对照、双盲、多中心的美国研究,主要评估VOQUEZNA在非糜烂... 查看详情
18
7月
FDA授予Ebvallo(Tabelecleucel)治疗成人和儿童EBV+移植后淋巴增生性疾病优先审查资格
2024年,美国食品药品监督管理局(FDA)接受了一项生物制品许可申请(BLA),旨在批准tabelecleucel(tab-cel)作为单药疗法,用于治疗2岁及以上的儿童和成人患者,这些患者在经历至少一次治疗后,仍然患有EBV(Epstein-Barr病毒)阳性移植后淋巴增生性疾病(PTLD)。此外,FDA还为此申请授予了优先审查资格,目标审查日期定为2025年1月15日。 无其他获批疗法下的突破 目前,FDA尚未批准任何治疗EBV阳性PTLD的药物。此次申请的支持数据来源于430多名患有多种危及生命疾病的患者,这些患者接受了tab-cel的治疗,包括关键的3期ALLELE试验(NCT033... 查看详情
18
7月
乌帕替尼Rinvoq用于儿童多关节幼年特发性关节炎和银屑病关节炎获FDA批准
2024年6月4日,美国食品药品监督管理局(FDA)正式批准了Janus激酶(JAK)抑制剂Rinvoq(乌帕替尼,upadacitinib)用于治疗对一种或多种肿瘤坏死因子(TNF)阻断剂反应不充分或不耐受的2岁及以上儿童患者的活动性多关节幼年特发性关节炎(pJIA)和银屑病关节炎(PsA)。这标志着儿科关节炎治疗领域迎来了新的希望。 临床研究与批准依据 此次批准基于多项严格的临床研究和数据分析。upadacitinib在成人类风湿性关节炎(RA)和PsA中的良好对照研究,以及成人RA和PsA患者的药代动力学数据,为其在儿童PsA中的应用提供了重要支持。同时,pJIA的批准得益于一项开放性、... 查看详情
17
7月
FDA授予SLS009儿童急性髓细胞性白血病罕见儿科疾病认定
近年来,SLS009在治疗儿童急性髓细胞性白血病(AML)方面取得了显著进展。美国食品药品监督管理局(FDA)已经授予SLS009罕见儿科疾病认定(RPDD),这是对这一潜在革命性治疗方法的高度认可。SLS009不仅仅是一种新的药物,它代表了治疗儿童AML的新希望。 SLS009的独特优势 SLS009,也曾称为GFH009,是一种高度选择性的CDK9抑制剂。此前,FDA已经授予其孤儿药和快速通道认定,用于治疗这一适应症。作为一种潜在的首创和最佳的CDK9抑制剂,SLS009在治疗儿童AML方面显示出极大的潜力。 SELLAS公司的总裁兼首席执行官Angelos Stergiou博士表示:“继... 查看详情
17
7月
口服Targretin(bexarotene)治疗皮肤T细胞淋巴瘤在香港获批
近年来,皮肤T细胞淋巴瘤(CTCL)的治疗进展备受关注。这种罕见的恶性肿瘤主要影响皮肤,给患者带来极大的痛苦和挑战。香港近日迎来了一个新的治疗选择——口服Targretin(bexarotene),这一消息由其研发公司Main Life宣布,引起了医学界的广泛关注。 Targretin(bexarotene)在中国的首次商业化 Targretin(bexarotene)早在2024年初就在澳门获得批准,这标志着它首次在中国市场的商业化应用。这一里程碑不仅为澳门患者带来了福音,也为香港的CTCL患者提供了新的治疗希望。Main Life公司在新闻发布中表示,Targretin(bexaroten... 查看详情
17
7月
靶向放射药物ABD-147治疗广泛期小细胞肺癌获FDA快速通道资格
小细胞肺癌(SCLC)的治疗一直是医学界的重大挑战。针对这一难题,FDA近日授予新一代精确放射药物治疗ABD-147快速通道资格,用于治疗在铂类化疗后病情进展的广泛期小细胞肺癌患者。这一决定标志着SCLC治疗领域的重大进展。 ABD-147:高效靶向放射药物的创新 ABD-147是一种靶向放射性生物药物,设计目的是将强效的α放射性同位素锕-225精准递送至表达DLL3蛋白的实体肿瘤。DLL3是一种存在于神经内分泌肿瘤表面的蛋白质,但在非恶性细胞或组织中极少表达。该蛋白在肺部上皮细胞和神经内分泌细胞分化的发育和调节中起着关键作用。 在超过80%的某些类型的高级别神经内分泌癌症病例中,如SCLC,... 查看详情