20
6月
Skyrizi(Risankizumab)治疗溃疡性结肠炎获FDA批准
2024年6月18日,伊利诺伊州芝加哥北市——艾伯维(AbbVie)公司迎来了一个里程碑时刻。美国食品和药物管理局(FDA)正式批准Skyrizi(risankizumab)扩展其适应症,用于治疗中度至重度活动性溃疡性结肠炎的成人患者。这一批准不仅为溃疡性结肠炎(UC)患者带来了新的希望,也标志着Skyrizi在治疗多种免疫介导的炎症性疾病方面的又一重大进展。 Skyrizi的独特机制:IL-23特异性抑制剂 Skyrizi(risankizumab)是一种人源化的IgG1亚型单克隆抗体,通过与IL-23的p19亚基结合,选择性地拮抗IL-23。IL-23是一种重要的炎症因子,与多种慢性免疫疾... 查看详情
19
6月
FDA批准Vigafyde(氨己烯酸,vigabatrin)用于治疗婴儿痉挛症
在罕见疾病领域,寻找有效的治疗方案一直是医药界的重大挑战。尤其对于婴儿痉挛症(IS)这样的罕见且严重的癫痫类型,迫切需要安全且高效的药物来改善患者的生活质量。近日,Pyros制药公司宣布,其开发的Vigafyde™(氨己烯酸,vigabatrin)口服溶液获得了美国食品和药物管理局(FDA)的批准,成为十五年来首个用于治疗婴儿痉挛症的新药。这一突破性进展不仅为患者和家庭带来了新的希望,也标志着Pyros公司在罕见疾病药物研发方面的卓越成就。 Vigafyde™的批准与意义 FDA的批准与药物概述 Pyros制药公司近期宣布,FDA已经批准了Vigafyde™(vigabatrin)口服溶液。V... 查看详情
19
6月
免疫球蛋白Yimmugo治疗原发性体液免疫缺陷获FDA正式批准
在现代医学的不断发展中,治疗复杂的免疫系统疾病已成为可能。近日,Grifols旗下的子公司Biotest宣布,美国食品和药物管理局(FDA)正式批准了一款新药——Yimmugo(静脉注射人免疫球蛋白,human-dira)。这一药物的批准标志着原发性体液免疫缺陷(PI)患者将迎来新的治疗希望。 原发性体液免疫缺陷的概述 原发性免疫缺陷病(PID)是一组由于先天性免疫系统发育不良或遗传因素导致的免疫功能障碍性疾病。PID的发病机制涉及免疫器官、组织、细胞或分子的缺陷,导致患者的免疫功能不足。具体来说,原发性体液免疫缺陷(PI)是PID的一种,主要表现为患者体内抗体水平低下,易感染细菌、病毒等病原... 查看详情
18
6月
FDA批准Capvaxive(21价肺炎球菌结合疫苗)用于预防成人侵袭性肺炎球菌疾病
2024年6月17日,美国食品药品监督管理局(FDA)批准了一种名为Capvaxive的新疫苗,这是一种21价肺炎球菌结合疫苗,专门设计用于预防成人的侵袭性肺炎球菌疾病和肺炎球菌肺炎。这一里程碑不仅为成人的健康保护提供了新的工具,也代表了科学在预防严重细菌感染方面的重大进步。 Capvaxive的批准背景 FDA的批准过程 2024年6月17日,FDA批准了默沙东(MSD)公司研制的Capvaxive(V116)21价肺炎球菌结合疫苗。该疫苗针对以下适应症: 对18岁及以上的个体进行主动免疫,以预防由肺炎链球菌血清型引起的侵袭性疾病。 对18岁及以上的个体进行主动免疫,以预防由肺炎链球菌血清型... 查看详情
16
6月
XEOMIN(A型肉毒杆菌毒素)治疗下肢局部痉挛在瑞士获批
近年来,医疗科技的不断进步为全球患者带来了更为个性化和有效的治疗方案。2024年6月14日,Merz Group旗下子公司、神经毒素领域的领导者Merz Therapeutics再次取得了重大突破。瑞士国家药品和医疗产品授权和监管机构Swissmedic正式批准XEOMIN®(A型肉毒杆菌毒素,incobotulinumtoxinA)用于治疗下肢局部痉挛。这一批准标志着在治疗痉挛方面的又一重要进展,具有深远的意义。 XEOMIN®的全球认可与成就 多国批准:全球治疗标准的新高度 XEOMIN®的成功不仅限于瑞士,它已经在全球75多个国家获得批准,用于治疗各种痉挛性疾病。这些包括上肢和下肢痉挛、... 查看详情
15
6月
FDA批准度伐单抗(Imfinzi)联合化疗用于dMMR原发性晚期或复发性子宫内膜癌
近期,美国食品药品监督管理局(FDA)批准了度伐单抗(Imfinzi,Durvalumab)联合卡铂和紫杉醇用于治疗错配修复缺陷(dMMR)的晚期或复发性子宫内膜癌。这一决定基于DUO-E 3期临床试验(NCT04269200)的数据支持,该试验结果显示dMMR肿瘤患者在度伐单抗(Imfinzi)治疗组中的无进展生存期(PFS)显著延长。 临床试验数据的支持 DUO-E试验设计和参与者 DUO-E试验是一项全球性、双盲、安慰剂对照的3期临床试验,参与者年龄需至少为18岁,患有新诊断的晚期III/IV期或复发性子宫内膜癌。试验排除了肉瘤患者,并要求已知的MMR状态方可入组。患者被随机分为三组:度... 查看详情
15
6月
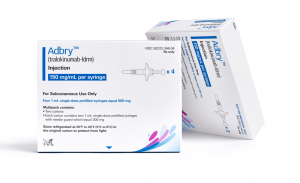
FDA批准新型Adbry(曲罗芦单抗)单剂量自动注射器治疗特应性皮炎
近日,利奥制药宣布了一项重磅消息:美国食品药品监督管理局(FDA)正式批准了一种新型单剂量自动注射器,用于其曲罗芦单抗(Adbry)的给药。这一新的设备预计将在未来几个月内上市,将为特应性皮炎患者带来更便捷的治疗选择。 Adbry:针对特应性皮炎的革命性治疗 一、作用机制 Adbry,即曲罗芦单抗(tralokinumab-ldrm),是一种白细胞介素13(IL-13)拮抗剂。IL-13是一种在特应性皮炎中起关键作用的细胞因子,驱动着与该病症相关的炎症过程。通过靶向并拮抗IL-13,Adbry可以有效减轻炎症,从而缓解特应性皮炎的症状。 二、适应症扩展 Adbry最初于2021年12月获得FD... 查看详情
15
6月
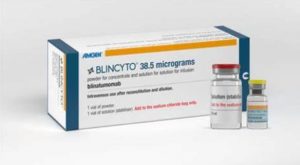
FDA批准Blincyto用于治疗CD19阳性、Ph阴性B细胞前体急性淋巴细胞白血病患者
在现代医学的飞速发展中,抗癌疗法不断取得重大突破。近日,美国食品药品监督管理局(FDA)批准了Blincyto(Blinatumomab)用于治疗CD19阳性、费城染色体(Ph)阴性、B细胞前体急性淋巴细胞白血病(B-ALL)的成人和儿童患者。这一决定基于一项重要的临床试验,显示了Blincyto(Blinatumomab)在提高患者生存率方面的显著效果。本文将详细介绍这一批准的背景、临床试验数据、患者特点及安全性数据。 FDA批准Blincyto(Blinatumomab)的背景 FDA此次批准Blincyto(Blinatumomab),适用于1个月及以上年龄的成人和儿童患者,目标群体为C... 查看详情
14
6月
FDA加速批准瑞普替尼Repotrectinib(Augtyro)用于NTRK基因融合阳性实体瘤
2024年6月,FDA宣布加速批准瑞普替尼(Augtyro,Repotrectinib)用于治疗12岁及以上的成人和儿童,这些患者的实体肿瘤含有NTRK基因融合,且病情已局部晚期或转移,或因手术切除可能导致严重并发症而不适合手术治疗,同时在接受治疗后病情进展或无其他满意治疗选择。这一决定标志着癌症治疗领域的又一次重要突破,为众多癌症患者带来了新的希望。 研究背景与TRIDENT-1试验 研究背景 瑞普替尼(Augtyro)是一种口服的小分子酪氨酸激酶抑制剂,主要用于靶向NTRK基因融合。FDA的此次批准基于TRIDENT-1试验的数据支持,这是一项多中心、单臂、开放标签、多队列的临床试验。试验... 查看详情
14
6月
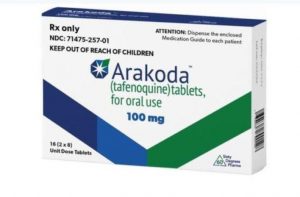
FDA批准Tafenoquine作为孤儿药用于治疗急性巴贝虫病
2024年6月11日,60度制药公司宣布美国食品和药物管理局(FDA)正式批准他非诺喹(tafenoquine)作为孤儿药用于治疗急性巴贝虫病。这一消息为许多受这种罕见疾病困扰的患者带来了新的希望。 急性巴贝虫病:一种被忽视的威胁 巴贝虫病的基本概况 急性巴贝虫病是一种由巴贝虫寄生虫引起的罕见传染病,主要通过黑腿(鹿)蜱的叮咬传播。这种疾病通过感染人体红细胞,导致溶血性贫血,症状包括发热、发冷、头痛、肌肉疼痛和疲劳等。在老年人和免疫系统较弱的人群中,巴贝虫病的感染可能会危及生命。 病原体与传播途径 巴贝虫病的主要传播媒介是黑腿蜱,这种蜱虫通常寄生在野生动物身上。蜱虫叮咬人类时会将寄生虫传染给宿... 查看详情