05
1月
重症肌无力新药Zilbrysq(zilucoplan)在美国上市
重症肌无力(gMG)是一种罕见而严重的免疫系统性疾病,患者可能面临全身肌肉无力和疲劳。近日,全球生物制药公司优时比(UCB)带来了一个令人振奋的消息,其创新药物Zilbrysq(zilucoplan)已成功在美国上市。这款药物的到来标志着科学家们在gMG治疗领域迈出了重要的一步,为患者提供了更便捷且有效的治疗方式。 1. Zilbrysq背后的创新技术 Zilbrysq是一种自我给药的C5补体抑制剂,成为美国食品药品监督管理局(FDA)批准的第一个、也是唯一一个自我给药的C5补体抑制剂,用于治疗抗乙酰胆碱受体(AChR)抗体阳性的成年患者的全身性重症肌无力(gMG)。这一创新技术的引入为gMG... 查看详情
05
1月
口服疗法Mitapivat或将为非输血依赖性地中海贫血带来新的曙光
地中海贫血,一种遗传性小细胞性溶血性贫血,常导致贫血、虚弱和疲乏等症状。而非输血依赖性地中海贫血则是一类无需常规输血或仅在特殊情况下需要输血的地贫类型。迄今为止,尚未有FDA批准的非输血依赖型地中海贫血的口服疗法。然而,最新研究表明,Agios Pharmaceuticals公司的Mitapivat或将成为该领域的先驱。 1. Mitapivat在非输血依赖性地中海贫血的突破性研究 最近,Agios Pharmaceuticals公司发布了Mitapivat在全球范围内进行的3期ENERGIZE研究的重大突破,该研究覆盖了非输血依赖性α-或β-地中海贫血成人。这一研究取得了令人振奋的成果,为M... 查看详情
04
1月
FDA授予DOC1021治疗恶性神经胶质瘤的孤儿药资格
医学领域的不断创新推动着癌症治疗的进步,而在这不懈的努力中,DOC1021作为治疗恶性胶质瘤的细胞疗法迈出了关键的一步。美国食品药品监督管理局(FDA)授予DOC1021孤儿药品认定,为其在恶性胶质瘤领域的疗效打开了更为广阔的可能性。本文将深入分析DOC1021的独特之处、研究结果以及未来前景,展现这一细胞疗法给恶性胶质瘤患者带来的新希望。 DOC1021的独特之处 DOC1021是一种独特的疫苗,由患者的树突状细胞和其肿瘤样本制成。通过使用树突状细胞,可以在不对患者免疫细胞进行基因修饰的情况下,精准地针对完整的癌症抗原。此外,这种疫苗利用了自然的免疫反应,可以像对待病毒感染一样,针对并清除癌... 查看详情
04
1月
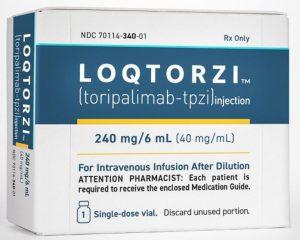
新一代鼻咽癌药物Loqtorzi在美国推出
随着医学研究和药物研发的不断进步,鼻咽癌患者有望迎来新的治疗时代。最新批准上市的药物Loqtorzi(toripalimab-tpzi,特瑞普利单抗)在美国上市,为成人转移性或复发性局部晚期鼻咽癌(NPC)的治疗提供了新的选择。 Loqtorzi的作用机制 Loqtorzi是一种程序性死亡受体-1(PD-1)单克隆抗体,具有针对鼻咽癌的独特作用机制。它通过调节免疫系统的活性,对抗癌细胞,为患者提供了一种全新的治疗途径。 临床试验结果 Loqtorzi的批准基于两项关键临床试验的结果:JUPITER-02试验和POLARIS-02研究。在JUPITER-02研究中,Loqtorzi与化疗联合使用... 查看详情
03
1月
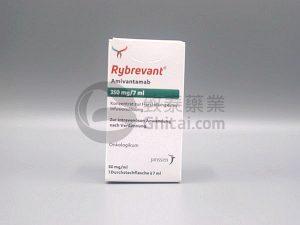
FDA将审查Rybrevant(amivantamab-vmjw)用于NSCLC亚群的潜在批准申请
近日,强生公司(Johnson & Johnson)向美国食品和药物管理局(FDA)提交了关于Rybrevant(amivantamab-vmjw)和lazertinib联合应用的两个独立申请,旨在争取其在EGFR基因exon 19缺失或L858R替代突变的局部晚期或转移性非小细胞肺癌(NSCLC)患者中的一线治疗获批。这一新疗法的前景令人瞩目,有望填补目前EGFR突变NSCLC患者治疗领域的不足。 试验结果支持 强生公司通过一份新闻稿宣布,他们已向FDA提交了一份补充生物制品许可申请和一份新药申请,以推动Rybrevant和lazertinib的联合应用获批。这一决定得到了MARIP... 查看详情
03
1月
FDA授予Aglatimagene Besadenovec+Valacyclovir治疗胰腺癌的快速通道地位
胰腺癌是一种具有高度侵袭性和低预后的癌症类型,迄今为止,对于这一疾病的治疗仍然是一项巨大的挑战。然而,一项新的临床研究带来了令人振奋的消息:美国食品和药物管理局(FDA)已授予Aglatimagene Besadenovec联合Valacyclovir用于胰腺导管腺癌(PDAC)的快速通道地位。这一决定标志着一种全新的治疗策略正在迅速推进,为胰腺癌患者带来了新的希望。 Aglatimagene Besadenovec及其机制 Aglatimagene Besadenovec(CAN-2409)是一种腺病毒复制缺陷的工程基因构造,其中包含了单纯疱疹病毒(HSV)衍生的胸腺嘧啶激酶基因。这种离体疗... 查看详情
03
1月
Arimoclomol针对C型尼曼匹克病的新药申请重新向美国FDA提交
2023年12月22日,Zevra Therapeutics,一家致力于罕见病治疗的公司,为其对抗尼曼匹克病C型(NPC)的使命取得了重要的里程碑。该公司自豪地宣布已经再次向美国食品和药物管理局(FDA)提交了Arimoclomol的新药申请(NDA)。这一研究中的治疗候选药物对于解决这种罕见而致命的神经系统疾病的未满足医学需求具有巨大的潜力。随着制药界急切期待FDA的回应,Zevra致力于推进患者护理的决心依然坚定不移。 I. Arimoclomol NDA再次提交:勤奋工作的胜利 Zevra Therapeutics表达了为Arimoclomol的NDA再次提交提供全面和高质量工作的坚定承... 查看详情
02
1月
CLS001荣获美国FDA孤儿药品认定
在医学科技领域的不断创新中,Cellusion Inc.于2023年12月22日宣布,其创始人兼首席执行官Shin Hatou博士医学博士学位(M.D. Ph.D.)领导的深科技初创公司取得了里程碑式的成就。美国食品药品监督管理局(FDA)正式授予Cellusion的再生医学产品“iPS细胞衍生的角膜内皮细胞替代物”(CLS001)孤儿药品认定(ODD),用于治疗大泡性角膜病变(bullous keratopathy)。这一认定不仅是对Cellusion科技实力的认可,也将为患有罕见疾病的患者带来曙光。 孤儿药品认定:FDA的嘉奖 美国FDA授予孤儿药品认定的前提是药物必须符合特定标准,主要用... 查看详情
02
1月
Zerpidio(斯鲁利单抗)治疗广泛期小细胞肺癌在印尼获批
在医学领域的不断创新与进步中,复宏汉霖近日宣布,其自主研发和生产的重组人源化抗PD-1单抗斯鲁利单抗(Serplulimab)于2023年12月28日成功获得印度尼西亚食品药品监督管理局(BPOM)的批准,用于治疗广泛期小细胞肺癌(ES-SCLC)。这标志着Zerpidio®在斯鲁利单抗首次成功获批上市,为肺癌患者带来了新的治疗选择。 2019年,复宏汉霖与合作伙伴PT Kalbe Genexine Biologics(KGbio)签署独家许可协议,授予KGbio在东盟十国的部分适应症及疗法的独家开发和商业化权利。随着时间的推移,公司进一步扩大与KGbio的合作范围,涵盖了中东和北非地区(ME... 查看详情
31
12月
抗癌药物多塔利单抗Jemperli(dostarlimab)的安全性研究获CDSCO小组批准
在药物研发领域,突破性的抗癌药物一直备受瞩目。最近,制药巨头葛兰素史克成功获得印度中央药品标准控制组织(CDSCO)下的专家小组批准,以开展抗癌药物多塔利单抗Jemperli(dostarlimab)的第四期临床试验。这一决定对于深化我们对该药物安全性的了解具有重要意义。 药物简介与研究提议 多塔利单抗Jemperli(dostarlimab),作为一种抗PD-1单克隆抗体,广泛应用于治疗失配修复的子宫内膜癌和无其他替代治疗选择的实体瘤。该药物的研究提案涉及进行第四期临床试验,旨在评估Jemperli(dostarlimab)在印度成年失配修复(dMMR)/微卫星不稳定高(MSI-H)复发性或... 查看详情