29
12月
FDA批准恩诺单抗PADCEV与KEYTRUDA联合治疗晚期膀胱癌
在美国食品和药物管理局(FDA)的授权下,辉瑞公司与爱力根公司自豪地宣布PADCEV®(enfortumab vedotin-ejfv,恩诺单抗),一种抗体药物结合物(ADC),与PD-1抑制剂KEYTRUDA®(pembrolizumab)联合使用,已获批用于成年患有局部晚期或转移性尿路上皮癌(la/mUC)的患者。这一批准标志着先进膀胱癌治疗领域的一个里程碑,为当前的标准治疗——含铂化疗的方法提供了一个引人注目的替代选择。 药物细节 PADCEV是一种首创的ADC,针对在膀胱癌中高表达的Nectin-4蛋白,通过将抗肿瘤剂单甲基金刚烷E(MMAE)内化并释放到细胞中,诱导细胞周期停滞和程序... 查看详情
29
12月
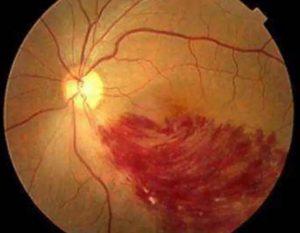
湿性AMD治疗新篇章:贝伐珠单抗眼科制剂Lytenava将展开非劣效性研究
在医学领域的不断进步中,Outlook Therapeutics生物制剂公司宣布将对其眼科制剂Lytenava进行一项为期三个月的非劣效性研究,以探索其在湿性年龄相关性黄斑变性(AMD)治疗中的潜力。 Lytenava眼科制剂简介 Lytenava,又名ONS-5010,是一种贝伐珠单抗眼科制剂,专为玻璃体内注射而设计。该制剂目前正等待FDA的特别方案评估,计划于2024年第一季度开始一项为期三个月的非劣效性研究。如果获得批准,Lytenava将成为唯一专门治疗年龄相关性黄斑变性的贝伐珠单抗产品。 贝伐珠单抗的作用机制 贝伐珠单抗是一种重组人源化单克隆抗体,属于血管内皮生长因子(VEGF)抑制... 查看详情
28
12月
Yescarta美国标签更新为大B细胞淋巴瘤患者带来曙光
近日,美国食品药品监督管理局(FDA)迈出了医学领域的一大步,正式批准了Yescarta (axicabtagene ciloleucel,阿基仑赛注射液) 处方信息的更新。这项更新将大B细胞淋巴瘤(LBCL)的总体生存数据纳入Yescarta的治疗效果评估中。这标志着基因修饰自体T细胞免疫疗法在肿瘤治疗领域的巨大进展,为患有复发性或难治性大B细胞淋巴瘤的患者带来了曙光。 新时代的治疗方法:Yescarta的独特之处 Yescarta由美国吉利德子公司Kite开发,是一种CD19导向的基因修饰自体T细胞免疫疗法,适用于成年患者,尤其是对一线化学免疫疗法难治性或在一线化疗后12个月内复发的大B细... 查看详情
27
12月
强生寻求FDA批准RYBREVANT(amivantamab)与Lazertinib治疗EGFR突变的非小细胞肺癌
2023年12月21日,强生公司宣布向美国食品和药物管理局(FDA)提交了RYBREVANT®(amivantamab-vmjw,埃万妥单抗)与Lazertinib联合用药的补充生物许可申请(sBLA)和新药申请(NDA),旨在获得对局部晚期或转移性表皮生长因子受体(EGFR)外显子19缺失或L858R替代突变的成年患者进行第一线治疗的批准,检测方法需通过FDA批准的检测。这一申请基于MARIPOSA阶段3研究的数据,标志着RYBREVANT®临床开发计划在四个月内的第三次提交,先前已提交了MARIPOSA-2和PAPILLON的sBLA。 RYBREVANT®与Lazertinib联合用药的... 查看详情
27
12月
欧盟委员会批准Vueway(gadopiclenol)的上市许可
德国康斯坦茨2023年12月22日电 /美通社/ — 2023年12月7日,欧盟委员会授予博莱科影像公司新型MR造影剂Vueway®(钆匹甲醇)上市许可。欧盟委员会的批准遵循了欧洲药品管理局 (EMA) 人用药品委员会 (CHMP) 的积极意见和 EMA 的建议。2024 年第一季度,Vueway® 也将在德国市场上市。 Vueway® – 下一代 MR 造影剂 Vueway® 是一种新型、高度稳定的钆基大环造影剂 (GBCA),用于对比增强磁共振成像。这是对 EMA 要求使用尽可能低量的钆的合乎逻辑的回应。与目前德国市场上的其他细胞外造影剂相比,Vueway® 的更高功效可以显着... 查看详情
27
12月
FDA已完成LUMAKRAS(Sotorasib)全面批准的补充新药申请的审查
2023年12月26日,Amgen公司宣布美国食品和药物管理局(FDA)完成了对其补充新药申请的审查,该申请旨在获得LUMAKRAS(Sotorasib)的全面批准。然而,这次审查却产生了一封完整回复信,审查基于CodeBreaK 200试验结果,该试验用于治疗先前接受治疗的局部晚期或转移性KRAS G12C突变的非小细胞肺癌(NSCLC)患者。FDA还发布了一项新的后市场要求(PMR),要求进行额外的确证研究以支持在最迟于2028年2月前完成的全面批准。 全面回应和新要求: FDA在审查中提出的关于LUMAKRAS加速批准时剂量比较的后市场要求已经得到满足。公司表示,LUMAKRAS在每日9... 查看详情
26
12月
吞下的振动胶囊或成控制体重的新选择
在追求健康的过程中,体重管理一直是人们关注的焦点。近期,研究人员开发了一种创新的振动胶囊,通过欺骗人体让胃产生饱腹感,为体重控制提供了新的选择。这种多维生素大小的胶囊在动物试验中显示,在进食前20分钟服用的动物摄食量比平时减少了约40%。 胶囊工作原理 这项技术由麻省理工学院的研究人员开发,利用了胃向大脑发出饱腹信号的过程,帮助人们意识到是时候停止进食了。胶囊的振动会激活胃中与感知饱腹有关的受体,就像胃充满食物而被拉伸的感觉一样。 因为胃内充满液体同样可以发送这些信号,这就解释了为什么节食者经常在用餐前喝一杯水。胶囊的振动模拟了胃被填充的感觉。 胶囊效果 研究发现,这种胶囊的振动会触发胃向大脑... 查看详情
25
12月
NICE对Rezurock(Belumosudil)治疗慢性移植物抗宿主病给予积极评价
在迈向医疗科技不断进步的道路上,新的治疗方案的出现为患者带来了新的曙光。近期,国家健康与护理卓越研究所(NICE)对Rezurock(Belumosudil)在慢性移植物抗宿主病(cGVHD)治疗中的积极意见,为患者提供了一项创新的治疗选择。本文将深入探讨Rezurock(Belumosudil)的重要性以及NICE的评价,为读者解读这一里程碑性的进展。 Rezurock(Belumosudil)的背景 Rezurock(Belumosudil)是一种治疗慢性移植物抗宿主病的新疗法,适用于12岁及以上的患者,这是英格兰和威尔士首个可用于已接受至少2线系统治疗的患者的疗法。该药物于2021年7月... 查看详情
24
12月
欧盟批准Rezzayo(Rezafungin)用于治疗侵袭性念珠菌病
近日,Mundipharma公司宣布令医学领域备受瞩目的消息:Rezzayo(Acetate Rezafungin)醋酸瑞扎芬净已成功获得欧盟(EU)的批准,将作为一项创新的治疗手段用于成人侵袭性念珠菌病。这一决定是在欧盟委员会(EC)积极审批后做出的,该审批基于人用药品委员会(CMUH)对ReSTORE III期临床试验的肯定意见。该试验结果表明,瑞扎芬净(Rezafungin)以每周一次的频率给药,其统计非劣效性超越了目前的护理标准卡泊芬净(Caspofungin)每天一次的给药方式。此外,这一决定也得到了II期STRIVE临床试验的积极结果和广泛非临床开发计划的全面支持。 治疗侵袭性念珠... 查看详情
23
12月
FDA优先审议Patritumab Deruxtecan在EGFR阳性NSCLC患者的治疗申请
肺癌是全球癌症发病率和死亡率的主要原因之一,而EGFR突变型非小细胞肺癌(NSCLC)患者的治疗一直备受关注。近期,美国食品和药物管理局(FDA)接受并优先审议了一项生物制剂许可申请(BLA),该申请旨在获得HER3-定向抗体药物复合物Patritumab Deruxtecan在成年患者中作为局部晚期或转移性EGFR突变型NSCLC的一线治疗的批准。 HERTHENA-Lung01试验结果支持优先审议 这一决策得到了来自HERTHENA-Lung01试验的数据支持。该试验包括先前接受至少两种系统治疗的EGFR激活突变的局部晚期或转移性NSCLC患者。试验结果显示,Patritumab Deru... 查看详情