04
2月
FDA授予T细胞疗法BST02快速通道资格用于治疗各种形式的肝癌患者
FDA授予BST02快速通道资格,用于所有形式的肝癌患者。 BST02 是一种使用患者自身免疫细胞的肿瘤浸润淋巴细胞 (TIL) 疗法,已获得 FDA 对所有形式的肝癌的快速通道指定。 这标志着TIL疗法在全球首个进入临床阶段的重大进展。 BST02在中国正在进行的1期试验(NCT06173726)正在招募晚期肝癌患者。 T细胞疗法BST02已获得FDA的快速通道认定,用于治疗各种形式的肝癌患者,包括肝细胞癌(HCC)和胆管癌患者。 此前在2023年10月,BST02在药物审评中心批准了一项研究性新药申请,用于1/2期临床试验的评估。2024年1月,BST02也获得了中国国家药品监督管理局的批... 查看详情
03
2月
FDA优先审查Afami-cel治疗晚期滑膜肉瘤的生物制品许可申请
近日,Adaptimmune Therapeutics公司宣布美国FDA已接受其生物制品许可申请(BLA),并给予其针对Afami-cel疗法的优先审评资格。Afami-cel是一种工程化T细胞疗法,针对治疗罕见而高度恶性的晚期滑膜肉瘤。如果获得批准,这将是首个用于治疗实体瘤的工程化T细胞疗法,也是十多年来治疗滑膜肉瘤的首个有效疗法。 滑膜肉瘤:一种罕见而具侵袭性的软组织肉瘤 滑膜肉瘤是一种罕见的高度恶性软组织肉瘤,主要发生在关节附近软组织。在肿瘤分类中,软组织肉瘤有50多种不同类型,其中滑膜肉瘤约占所有软组织肉瘤的5%至10%。目前,手术仍然是滑膜肉瘤的首选治疗方法,然而,切除不彻底可能导致... 查看详情
02
2月
寻常痤疮新药Cabtreo外用凝胶在美国上市
在医学和美容领域的不断创新中,治疗和管理皮肤问题的产品不断涌现。近日,Bausch Health和Ortho Dermatologics携手推出的Cabtreo外用凝胶成为焦点,该产品不仅是美国FDA批准的首款,也是唯一一款每日一次的固定剂量三联外用治疗寻常痤疮的产品。 Cabtreo的独特成分及治疗机制 Cabtreo外用凝胶的特殊之处在于其含有克林霉素磷酸酯、阿达帕林和过氧化苯甲酰这三种成分。克林霉素磷酸酯是一种半合成抗生素,阿达帕林则是一种合成的类视黄醇,而过氧化苯甲酰则是一种具有杀菌和角质溶解作用的氧化剂。这三者被结合到一种局部凝胶中,构成了治疗痤疮的独特组合。该产品成为首个每日一次的... 查看详情
02
2月
抗真菌药物Avycaz适用年龄扩大纳入3个月以内的儿科患者
在医学领域的不断创新和研究中,药物的适用范围不断得到扩展,以更好地满足患者的需求。最近,美国食品药品监督管理局(FDA)作出了一项重要的决定,将抗真菌感染药物Avycaz(ceftazidime-avibactam,头孢他啶和阿维巴坦)的适用年龄扩大,纳入了从出生到3个月以内的儿科患者。这一决策的背后是一项综合而深入的研究,旨在确保婴儿和幼儿在面对复杂感染时能够获得更全面、有效的治疗。 药物背景及历史 Avycaz,又名ceftazidime-avibactam,是一种用于治疗复杂腹腔感染(cIAI)、复杂性尿路感染(cUTI)以及医院获得性细菌性肺炎和呼吸机相关性细菌性肺炎(HABP/VAB... 查看详情
01
2月
FDA授予Liso-Cel(Breyanzi)用于MCL和FL中的优先审查申请
白血病和淋巴瘤等血液恶性肿瘤一直是医学领域关注的焦点。近日,美国食品药品监督管理局(FDA)以及日本卫生劳动与福祉省宣布,非常有前景的嵌合抗原受体(CAR)T细胞疗法Liso-Cel(Breyanzi)已获得在复发/难治性滤泡性淋巴瘤(FL)和纹状细胞淋巴瘤(MCL)中的优先审查资格。这一决定将极大推动该疗法在全球范围内的应用。 优先审查批准 FDA和日本卫生劳动与福祉省已经同意对Liso-Cel(Breyanzi)进行补充生物许可申请(sBLAs)的优先审查,覆盖了复发/难治性滤泡性淋巴瘤(FL)和纹状细胞淋巴瘤(MCL)的治疗。美国FDA的目标行动日期定为2024年5月23日,而日本的审查... 查看详情
01
2月
FDA批准Axi-cel(Yescarta)制造工艺变更,缩短等待时间
治疗急性髓系白血病(AML)是医学界长期追求的目标之一。近日,美国食品药品监督管理局(FDA)批准了Axi-cel(Yescarta)的制造工艺变更,从而缩短了平均生产周期。这一变革将使患者能够更快获得Axi-cel治疗,有望提高治疗效果。 制造工艺变更的批准 FDA已经批准Axi-cel(Yescarta)的制造工艺变更,从而将预期的生产周期从16天缩短至14天。这个周期是指从患者T细胞收集(白细胞分离)开始,到最终治疗产品准备好进行输注的时间。制造工艺对于个体化细胞治疗至关重要,特别是在这个时间范围内。 Cindy Perettie,吉利德公司下属Kite公司的执行副总裁,在新闻发布会上表... 查看详情
31
1月
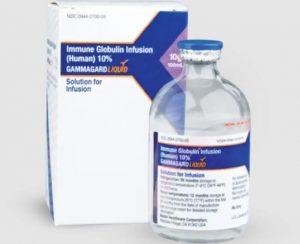
FDA批准Gammagard Liquid用于治疗慢性炎性脱髓鞘性多发性神经病
在医学科技不断进步的时代,药物的不断研发和批准为罕见病种的治疗提供了新的可能性。最新消息显示,武田制药公司的Gammagard Liquid(免疫球蛋白输注10%)已经获得美国食品药品监督管理局(FDA)的批准,用于治疗慢性炎性脱髓鞘性多发性神经病(CIDP)。这一新的药物批准标志着对CIDP患者的治疗选择范围的拓展,将为这一罕见神经肌肉疾病的患者带来新的希望。 CIDP的挑战与治疗需求 CIDP是一种罕见的神经肌肉疾病,其特征是逐渐恶化的神经系统症状,如四肢无力、刺痛、感觉丧失等。由于CIDP的症状可能与其他神经肌肉疾病重叠,导致误诊的可能性较大。传统上,免疫球蛋白疗法被认为是CIDP的有效... 查看详情
31
1月
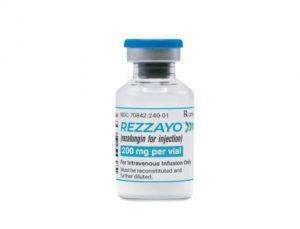
抗真菌药物REZZAYO(rezafungin,瑞扎芬净)治疗侵袭性念珠菌病在英国获批
在医学领域,不断涌现的药物批准为各种疾病的治疗提供了新的可能性。最近,英国药监机构MHRA批准了一款抗真菌药物REZZAYO(rezafungin,瑞扎芬净)用于治疗侵袭性念珠菌病,这为患者带来了新的希望。 REZZAYO(瑞扎芬净)的批准意义 侵袭性念珠菌病是由念珠菌引起的一种严重感染,可能影响多个器官系统,对患者的健康构成重大威胁。英国药监机构MHRA的批准意味着REZZAYO成为治疗这种感染的有效工具,为那些曾面临有限治疗选择的患者提供了新的希望。这一批准也证实了REZZAYO在美国FDA和欧盟委员会的批准后,在国际范围内的重要性。 侵袭性念珠菌病的临床背景 尽管一些常见的念珠菌感染相对... 查看详情
31
1月
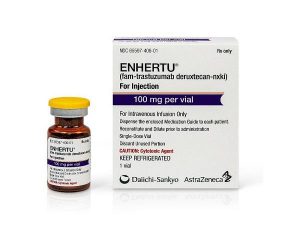
Enhertu(Trastuzumab Deruxtecan)治疗转移性HER2阳性实体瘤获FDA优先审查
在癌症治疗领域,新的药物研发和批准对患者而言是一线希望,特别是那些面临转移性实体瘤挑战的患者。近日,一款针对HER2阳性实体瘤的新药Trastuzumab Deruxtecan(Enhertu)取得FDA优先审查的好消息,为患者提供了新的治疗选择。本文将深入探讨该药物的研发背景、临床试验数据以及对癌症治疗领域的积极影响。 FDA优先审查批准 昨日,美国食品药品监督管理局(FDA)宣布同意优先审查Enhertu(Trastuzumab Deruxtecan)的补充生物制剂许可申请(sBLA)。该药物的适用范围将覆盖患有不可切除或转移性HER2阳性实体瘤的成年人,尤其是那些之前接受过治疗或未能获得... 查看详情
31
1月
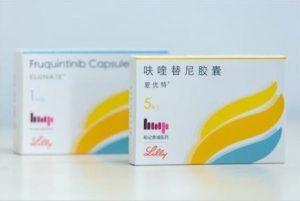
爱优特ELUNATE(呋喹替尼,fruquintinib)治疗转移性结直肠癌在香港获批
024年1月30日,和黄医药宣布旗下药物爱优特® (ELUNATE®, 呋喹替尼/fruquintinib) 获得香港药剂业及毒药管理局批准,正式用于治疗成年人转移性结直肠癌患者。这一消息为结直肠癌患者提供了新的治疗选择,呋喹替尼作为一种选择性口服抑制剂,将为那些曾接受过特定基础化疗和不适合接受抗血管内皮生长因子治疗的患者带来希望。 ELUNATE® (呋喹替尼)的治疗适应症扩展 呋喹替尼是一种血管内皮生长因子受体(VEGFR)1、2和3的选择性口服抑制剂。在获得香港批准后,该药物将用于治疗那些既往接受过氟尿嘧啶类、奥沙利铂和伊立替康为基础的化疗,以及既往接受过或不适合接受抗血管内皮生长因子 ... 查看详情