20
11月
TAKHZYRO(拉那利尤单抗)在欧盟获批用于儿童遗传性血管性水肿预防
2023年11月17日,武田公司宣布其创新药物TAKHZYRO®(lanadelumab,拉那利尤单抗)获得欧盟委员会批准,用于2岁及以上儿童遗传性血管性水肿(HAE)的常规预防。这一批准标志着欧洲经济区首个面向6岁以下儿童的HAE长期预防性治疗药物的诞生。 革命性的适应症扩展 儿科患者的常规预防 此前,TAKHZYRO®已获得欧盟批准用于12岁及以上患者的HAE复发性发作的常规预防。这次更新使其适用于2岁及以上的儿童,填补了这一年龄段HAE治疗的空白。这一决定的基础是对SHP643-301临床数据的支持,结合了关键的成人和青少年研究,以及新的150毫克预填充注射器配方的质量数据。 新的预防注... 查看详情
18
11月
VYVGART(艾加莫德α)获欧盟批准成为治疗全身性重症肌无力的新利器
2023年11月16日,免疫学公司argenx SE喜报频传,欧盟委员会(EC)正式批准VYVGART(efgartigimod alfa)皮下注射剂作为全身性重症肌无力(gMG)的标准疗法附加疗法,标志着该疾病领域的重大治疗突破。这一决定进一步拓展了VYVGART的应用范围,使其不仅适用于静脉注射,还可以通过自我管理的皮下注射实现治疗。 VYVGART的历程 在此之前,VYVGART IV已于2022年8月获得EC的批准。而这次的批准使VYVGART成为在欧洲27个成员国以及冰岛、挪威和列支敦士登等地自我管理的皮下注射治疗方案。argenx将与各地卫生当局密切合作,确保患者能够充分获得VYV... 查看详情
17
11月
FDA批准Truqap(Capivasertib)与Faslodex联合治疗晚期激素受体阳性/HER2阴性乳腺癌
在最新的决策中,美国食品药品监督管理局(FDA)已批准Capivasertib(Truqap)与Fulvestrant(Faslodex)联合治疗成年患者的乳腺癌。此次批准适用于激素受体阳性、HER2阴性、局部晚期或转移性乳腺癌,这些癌症患者携带了1个或多个PIK3CA、AKT1或PTEN基因改变,这些改变是通过FDA批准的检测方法检测到的,且患者在转移性情境中使用了至少一种基于内分泌的方案,或在辅助治疗结束后的12个月内出现了复发。 临床试验数据支持决策 这一决策基于CAPItello-291试验(NCT04305496)的数据,该试验是一项3期试验,纳入了708名携带PIK3CA/AKT1... 查看详情
17
11月
新一代糖尿病药物Mounjaro的新版本Zepbound获得FDA批准用于减肥
2023年,美国食品药品监督管理局(FDA)宣布,备受欢迎的糖尿病治疗药物Mounjaro的新版本现在可以作为减重药物销售。该新版本由爱力 Lilly 公司研发,名为Zepbound。这一药物,也被称为tirzepatide,在测试中帮助节食者减重40至60磅。 药物治疗成为糖尿病患者减重新选择 Zepbound是最新获得FDA批准用于慢性减重的糖尿病药物,与诺和诺德公司的Wegovy相似,后者是其糖尿病治疗药物Ozempic的高剂量版本。这两者均为每周注射。 FDA批准Lilly公司的药物用于被视为肥胖的人,其体质指数为30或更高,或者那些体重超标并伴随相关健康状况(如高血压、高胆固醇或糖尿... 查看详情
17
11月
Casgevy治疗镰刀型细胞贫血病和输血依赖性β地中海贫血在英国获批
医学领域的科技突破为许多罕见疾病患者带来了曙光,其中包括镰刀型细胞贫血病(SCD)和输血依赖性β地中海贫血(TDT)。在2023年11月16日,美国波士顿和瑞士楚格的Vertex Pharmaceuticals和CRISPR Therapeutics宣布,其颠覆性的CRISPR/Cas9基因编辑疗法Casgevy(exagamglogene autotemcel,exa-cel)已获得英国药品和健康产品管理局(MHRA)的有条件上市许可。这标志着Casgevy成为全球首款获批上市的CRISPR基因编辑疗法,为SCD和TDT患者带来新的治疗选择。 Casgevy的临床试验和成果 治疗SCD的突破... 查看详情
17
11月
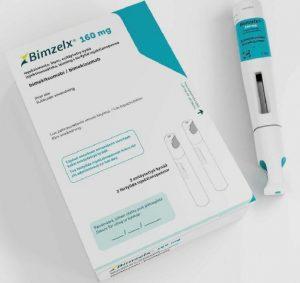
中重度斑块型银屑病治疗药物Bimzelx(比美吉珠单抗)在美国上市
在医学领域的不断创新中,全球生物制药公司优时比(UCB)于11月14日宣布了一项引人瞩目的消息——Bimzelx(bimekizumab-bkzx,比美吉珠单抗)已在美国成功上市。这一突破性的治疗药物针对中度至重度斑块型银屑病,为患者提供了一种新的治疗选择。本文将深入探讨Bimzelx的特点、机制以及基于临床试验的疗效和安全性。 Bimzelx的突破性特点 靶向治疗机制 Bimzelx通过皮下注射给药,是一种新型人源化单克隆IgG1抗体。其设计目标是阻断白细胞介素17A(IL-17A)和白细胞介素17F(IL-17F)这两种信号蛋白,这些蛋白负责推动斑块型银屑病中的炎症反应。与其他生物药物不同... 查看详情
17
11月
心血管药物Lepodisiran单剂皮下注射持续48周降脂蛋白(a)高达94%
在心血管疾病领域,一种名为Lepodisiran的新型药物近日引起了广泛关注。据最新研究结果显示,这种由礼来公司研发的siRNA药物在一项1期试验中表现出色,其单次注射在48周内将脂蛋白(a)水平降低高达94%。这一突破性的成果不仅为心血管疾病治疗提供了新的方向,也为那些与Lp(a)相关的健康问题提供了潜在的解决方案。 脂蛋白(a)与心血管疾病 脂蛋白(a),简称Lp(a),是一种在肝脏中产生的脂蛋白,与人体内的低密度脂蛋白(LDL)相似。不同于其他胆固醇微粒,Lp(a)的水平80-90%由基因决定。其异常水平与动脉斑块的积聚有关,从而显著增加心脏病发作和中风的风险。有研究估计,约50%的动脉... 查看详情
16
11月
DefenCath获FDA批准用于降低血液透析患者导管相关血流感染发生率
在生命威胁性疾病和状况的预防和治疗领域,生物制药公司CorMedix Inc.最近宣布其新药DefenCath®(牛磺罗定和肝素)导管锁定液(CLS)已获得美国食品药品监督管理局(FDA)批准,用于减少通过中心静脉导管(CVC)接受慢性血液透析的肾功能衰竭成年患者中导管相关的血流感染(CRBSIs)的发生率。DefenCath是美国第一款也是唯一一款FDA批准的抗微生物CLS,根据第3期临床研究显示,其可降低CRBSIs的风险高达71%。 背景与意义 肾功能衰竭患者,特别是那些通过CVC接受慢性血液透析的患者,一直以来都面临着导管相关的血流感染的威胁。这项FDA的批准意味着患者和医护人员在防范... 查看详情
16
11月
FDA批准Augtyro(repotrectinib)用于治疗ROS1阳性非小细胞肺癌
美国食品药品监督管理局(FDA)最近批准了Bristol Myers Squibb公司的新药Augtyro(repotrectinib),用于治疗成年患者的局部晚期或转移性ROS1阳性非小细胞肺癌(NSCLC)。这是一项创新的口服疗法,有望为患者带来新的希望。 了解Augtyro Augtyro是一种酪氨酸激酶抑制剂(TKI),以口服剂形式投放市场,主要针对ROS1致癌融合基因。该药物的批准基于TRIDENT-1研究,这是一项开放标签、单臂、1/2期试验,旨在评估Augtyro在TKI-naïve和TKI预处理患者中的疗效。研究结果显示,在TKI-naïve患者中,Augtyro的客观缓解率(... 查看详情
16
11月
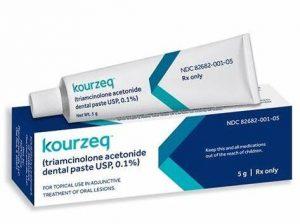
Kourzeq口腔牙膏亮相,缓解口腔溃疡的新选择
口腔溃疡作为一种常见口腔疾病,给患者带来了诸多痛苦。针对这一问题,MidAmerica Pharmaceuticals 推出了一款创新产品——Kourzeq口腔牙膏。作为FDA批准的处方口腔糊剂,Kourzeq致力于辅助治疗和缓解与外伤引起的口腔炎症性病变和溃疡性病变相关的症状。 Kourzeq:新一代口腔溃疡治疗方案 口腔溃疡,俗称口疮性溃疡,是一种发生在口腔软组织上的浅表病变。MidAmerica Pharmaceuticals 推出的Kourzeq口腔牙膏含有皮质类固醇曲安奈德,这一成分是治疗口腔病变的关键。尽管局部类固醇的确切机制尚不清楚,但皮质类固醇通过诱导磷脂酶A2抑制蛋白的作用,... 查看详情