24
11月
美国FDA批准PADCEV(维恩妥尤单抗)联合Keytruda用于肌层浸润性膀胱癌患者
PADCEV(Enfortumab vedotin,维恩妥尤单抗)联合Keytruda是首个且唯一获批的围手术期治疗方案,针对不适合顺铂治疗的肌层浸润性膀胱癌患者,相比当前标准治疗方案可显著改善生存期。 此项批准基于关键性III期EV-303试验取得的突破性数据。结果显示,与单纯手术相比,该联合方案可使疾病复发、进展或死亡风险降低60%,死亡风险降低50%。 这是针对该患者群体的首个且唯一的抗体偶联药物与PD-1抑制剂联合方案,有望成为新的标准治疗方案。 纽约和东京–辉瑞公司与安斯泰来制药今日共同宣布,美国食品药品监督管理局已批准PADCEV联合PD-1抑制剂Keytruda,作为... 查看详情
22
11月
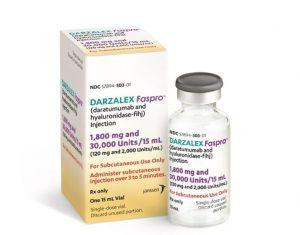
美国FDA批准Darzalex Faspro联合疗法用于轻链淀粉样变性治疗
11月19日,美国食品药品监督管理局正式批准达Darzalex Faspro(daratumumab and hyaluronidase-fihj,达雷妥尤单抗-透明质酸酶)联合硼替佐米、环磷酰胺和地塞米松(VCd)方案,用于治疗新诊断轻链淀粉样变性患者。此项决定将2021年基于加速审批途径获得的上市许可转为完全批准,主要依据来自III期ANDROMEDA研究的临床数据。 这项开放标签、随机、活性对照试验共纳入388名新诊断轻链淀粉样变性患者,所有患者均存在可测量病变且至少一个器官受累。研究按1:1比例随机分配患者接受VCd方案或Darzalex Faspro联合VCd方案治疗。根据在2024... 查看详情
21
11月
戈利木单抗生物类似药Gobivaz在欧盟获批
欧盟委员会已正式批准戈利木单抗生物类似药Gobivaz®在欧洲经济区上市。该药由Alvotech公司开发,是欧洲首个获批的Simponi®(golimumab,戈利木单抗)生物类似药。 Gobivaz®获批的剂型包括50 mg/0.5 mL和100 mg/mL两种规格,提供预充式注射器和自动注射器两种选择。 Gobivaz®获批用于治疗多种免疫介导的慢性炎症性疾病。 对成人患者,其适应症包括与甲氨蝶呤联合使用的类风湿关节炎、伴或不伴甲氨蝶呤的银屑病关节炎、轴性脊柱关节炎和溃疡性结肠炎。 对儿童患者,该药也可用于2岁及以上的幼年特发性关节炎患者,同样需要与甲氨蝶呤联合使用。 欧盟委员会的批准基于... 查看详情
21
11月
FDA批准地舒单抗生物类似药Osvyrti与Jubereq用于骨质疏松症/骨折高风险人群
美国食品药品监督管理局已批准denosumab-desu(商品名Osvyrti)与denosumab-desu(商品名Jubereq),分别对应参照药地舒单抗(商品名Prolia)与参照药地舒单抗(商品名Xgeva)的全部适应症。Osvyrti适用于骨质疏松症及相关骨病治疗,Jubereq则专注于肿瘤相关的骨骼疾病治疗,二者的临床定位与参照药Prolia和Xgeva保持一致。 Osvyrti的适应症包括:治疗骨折高风险绝经后女性骨质疏松症;提高骨折高风险男性骨质疏松症患者的骨量;治疗骨折高风险糖皮质激素诱导性骨质疏松症的男女性患者;提升接受雄激素剥夺治疗的非转移性前列腺癌高风险骨折男性的骨量;... 查看详情
21
11月
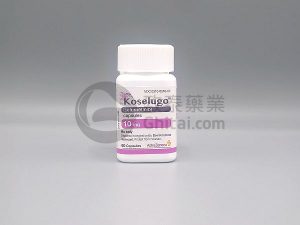
Koselugo(司美替尼)获美国批准用于1型神经纤维瘤病(NF1)丛状神经纤维瘤
基于KOMET III期临床试验结果,Koselugo(selumetinib,司美替尼)获得美国食品药品监督管理局批准,用于治疗伴有症状性、无法手术的丛状神经纤维瘤(PN)的1型神经纤维瘤病(NF1)成人患者。该试验数据显示,治疗组肿瘤体积缩小的总体缓解率达到20%。 KosETUGO是一种口服选择性MEK抑制剂。此次获批依据的是KOMET试验的积极结果,这是该患者群体中规模最大且唯一设置安慰剂对照的全球III期临床试验。相关数据已在2025年美国临床肿瘤学会年会公布,并发表于《柳叶刀》。 NF1是一种罕见的进行性遗传疾病,通常在儿童早期确诊,但常会持续进展至成年期,可能累及全身所有器官系统... 查看详情
21
11月
美国FDA加速批准Hyrnuo(sevabertinib)用于晚期HER2突变非小细胞肺癌患者
加速批准基于SOHO-01 I/II期试验数据:在未接受过HER2靶向治疗的患者中客观缓解率达到71%(N=70)。该研究中sevabertinib展现出持续的抗肿瘤活性及可控的安全性特征。HER2突变非小细胞肺癌通常预后较差且治疗选择有限。 2025年11月20日,经过优先审评并基于突破性疗法认定,美国食品药品监督管理局已加速批准Hyrnuo™(sevabertinib)用于治疗经FDA批准检测方法确认携带人表皮生长因子受体2(HER2)酪氨酸激酶域激活突变、且既往接受过全身治疗的局部晚期或转移性非鳞状非小细胞肺癌成人患者。Sevabertinib是一种口服可逆小分子酪氨酸激酶抑制剂。 此项... 查看详情
20
11月
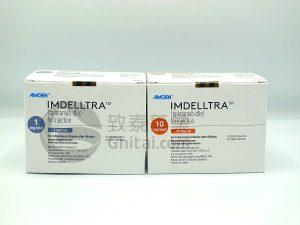
美国FDA全面批准IMDELLTRA(塔拉妥单抗)用于广泛期小细胞肺癌治疗
全球验证性三期DeLLphi-304试验显示,与化疗相比,IMDELLTRA可降低死亡风险40% 该批准确认IMDELLTRA成为广泛期小细胞肺癌疾病进展后公认的标准治疗方案 安进(Amgen)公司宣布,美国食品药品监督管理局已全面批准IMDELLTRA(Tarlatamab-dlle,塔拉妥单抗)用于治疗接受铂类化疗后疾病进展的广泛期小细胞肺癌成年患者。这一决定基于全球三期DeLLphi-304研究的数据,将IMDELLTRA之前的加速批准转为全面批准。此外,美国国家综合癌症网络临床实践指南近期更新,将tarlatamab列为唯一1类优选治疗方案,适用于铂类化疗后疾病进展的广泛期小细胞肺癌成... 查看详情
20
11月
美国FDA批准Redemplo(plozasiran)用于家族性乳糜微粒血症综合征治疗
Redemplo(plozasiran)是一种小干扰RNA药物,作为饮食辅助手段,用于降低家族性乳糜微粒血症综合征(FCS)成人患者的甘油三酯水平。FCS是一种严重罕见疾病,美国约有6500名遗传性或临床诊断的FCS患者。该疾病以甘油三酯水平异常升高为特征,可达正常值的10至100倍,显著增加急性、复发性和潜在致命性胰腺炎的发生风险。 Redemplo是首个且唯一获得FDA批准用于FCS患者的小干扰RNA药物,可通过皮下注射每三个月一次自行给药。该药物采用专有的靶向RNAi分子技术平台,是其研发公司获得FDA批准的首个药物。 FDA批准基于三期PALISADE研究的积极结果。这项随机、双盲、安... 查看详情
19
11月
Remsima(英夫利西单抗)IV静脉注射液制剂欧盟获批
欧洲委员会已批准Remsima™IV(静脉注射)液体配方,该产品是全球首个英夫利西单抗(Infliximab)静脉输注液剂,其适用范围涵盖此前Remsima™静脉输注粉剂的所有获批适应症。 本次批准基于英夫利西单抗粉剂与液剂之间的可比性研究数据。新推出的液剂规格包括100毫克及新增的350毫克,无需复溶步骤,使药物准备时间缩短51%,相关准备成本降低20%。 根据在七个欧洲国家的测算,预计每年可节约高达260万欧元的成本,同时显著提升工作流程效率。 Remsima™静脉输注液剂在欧盟获准用于所有英夫利西单抗静脉制剂的适应症,包括类风湿关节炎、成人与儿童克罗恩病、溃疡性结肠炎、儿童溃疡性结肠炎、... 查看详情
19
11月
欧盟批准Brinsupri(Brensocatib)用于非囊性纤维化支气管扩张症治疗
2025年11月18日,Insmed Incorporated今日宣布,欧盟委员会已批准Brinsupri(Brensocatib 25毫克片剂)用于治疗12岁及以上、过去12个月内发生两次或以上急性加重的非囊性纤维化支气管扩张症患者。Brinsupri是首款针对该疾病的创新疗法,也是欧盟范围内首个且唯一获批用于NCFB的治疗方案。基于其对公共卫生的重要价值,该药物通过了欧洲药品管理局的加速评估程序。 NCFB是一种慢性进行性疾病,可导致永久性肺损伤和肺功能下降。与其他以气道狭窄为特征的呼吸系统疾病不同,支气管扩张症患者的气道会永久性扩大,导致黏液和细菌更难以清除,从而引发持续性炎症和感染。该... 查看详情