26
2月
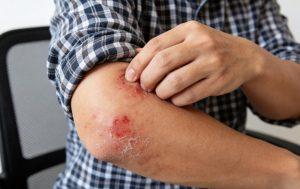
美国FDA批准Adquey(地法米司特1%)用于轻中度特应性皮炎治疗
2026年2月13日,Acrotech Biopharma Inc.宣布,美国食品药品监督管理局已批准非类固醇类药物Adquey(difamilast 1%,地法米司特1%)软膏的新药申请,用于局部治疗2岁及以上成人和儿童患者的轻中度特应性皮炎。 Adquey是一种新型非甾体类局部用磷酸二酯酶4(PDE4)抑制剂,对所有磷酸二酯酶4亚型均显示出抑制活性。其作用机制为通过抑制PDE4的活性,导致细胞内环磷酸腺苷积累,减少多种细胞因子和趋化因子的产生,改变细胞信号传导并降低皮肤中的炎症信号,从而缓解特应性皮炎相关症状,但其发挥治疗作用的具体机制尚不完全明确。 Adquey为局部用软膏剂型,仅供皮肤... 查看详情
25
2月
FDA完全批准Braftovi联合Erbitux及化疗用于BRAF V600E突变转移性结直肠癌
FDA已正式批准Braftovi(encorafenib,康奈非尼/恩考芬尼)联合Erbitux(Cetuximab,西妥昔单抗)及含氟尿嘧啶的化疗方案,用于经FDA批准的检测方法确认为携带BRAF V600E突变的成年转移性结直肠癌患者。 该监管决定基于3期BREAKWATER试验的临床数据。在该试验中,接受Braftovi联合Erbitux及mFOLFOX6方案治疗的B组患者,总缓解率达到61%,而接受含或不含贝伐珠单抗化疗的C组患者总缓解率为40%,两组差异具有统计学意义。B组中位无进展生存期为12.8个月,C组为7.1个月,疾病进展或死亡风险降低47%。B组中位总生存期为30.3个月,... 查看详情
25
2月
美国FDA批准Loargys(Pegzilarginase)用于患有精氨酸酶1缺乏症的高精氨酸血症治疗
2026年2月23日,Immedica Pharma宣布,美国食品药品监督管理局已加速批准Loargys,其活性成分为Pegzilarginase,用于联合饮食蛋白限制,治疗2岁及以上成人和儿童精氨酸酶1缺乏症患者的高精氨酸血症。 Loargys是一种经钴取代的重组人精氨酸酶1酶,与5 kDa甲氧基聚乙二醇载体共价结合,每摩尔蛋白质的取代度为6-12摩尔甲氧基聚乙二醇,结合后蛋白质的分子量约为224-344 kDa。甲氧基聚乙二醇载体可降低Loargys的清除率,延长其半衰期,同时维持酶的功能。该药品旨在替代精氨酸酶1缺乏症患者体内缺乏的人精氨酸酶1酶活性,可快速且持续地降低血浆精氨酸水平,并... 查看详情
24
2月
FDA授予Rybrevant Faspro(艾万妥单抗皮下注射剂)治疗晚期头颈部鳞癌突破性疗法认定
Rybrevant Faspro单药疗法获FDA突破性疗法认定,用于治疗复发或转移性、非HPV相关的头颈部鳞状细胞癌。 FDA已授予Amivantamab与透明质酸酶联合皮下注射制剂(Rybrevant Faspro;艾万妥单抗皮下注射剂)突破性疗法认定,作为单药治疗接受含铂化疗及PD-L1或PD-1抑制剂治疗后疾病进展的复发或转移性、非人乳头瘤病毒(HPV)相关的头颈部鳞状细胞癌(HNSCC)成人患者。 此项监管决定基于1b/2期OrigAMI-4研究(NCT06385080)队列1的数据,该数据已在2025年ESMO大会上公布。中位随访8.3个月(范围1.1-13.4)时,疗效可评估人群(... 查看详情
24
2月
欧盟批准Exdensur(Depemokimab)用于重度哮喘和伴有鼻息肉的慢性鼻窦炎
葛兰素史克(GSK)于2026年2月17日宣布,欧盟委员会(EC)已批准Exdensur(Depemokimab)上市 。这款药物获批的两个适应症分别为:作为添加维持治疗,用于治疗12岁及以上、以血嗜酸性粒细胞计数为特征的2型炎症重度哮喘成人及青少年患者;以及作为鼻用皮质类固醇的添加疗法,用于治疗成人重度伴有鼻息肉的慢性鼻窦炎(CRSwNP)患者 。 Exdensur是一款超长效生物制剂,其设计目标是通过抑制白细胞介素-5(IL-5)来发挥作用,IL-5是2型炎症中的关键细胞因子 。该药物的特点是具有较高的IL-5结合亲和力和效力,并结合了延长的半衰期,从而支持每六个月给药一次的方案 。这使得... 查看详情
21
2月
欧盟批准Akynzeo口服混悬液用于预防化疗相关恶心呕吐
2026年2月12日,欧洲委员会授予Akynzeo口服混悬液上市许可,该药品由赫尔辛医疗集团研发,其活性成分为奈妥匹坦和帕洛诺司琼,用于预防化疗引起的急性和迟发性恶心和呕吐。此次获批标志着Akynzeo产品组合的进一步扩展,为癌症患者提供了除现有获批剂型外的新治疗选择。 Akynzeo口服混悬液是一种固定组合止吐药,由神经激肽1受体拮抗剂奈妥匹坦和5-羟色胺3受体拮抗剂帕洛诺司琼组成,这两种成分通过同时抑制化疗引起的恶心和呕吐的两个关键通路,实现对急性和迟发性症状的预防。其中,5-羟色胺3受体拮抗剂被认为是预防化疗后24小时内(即急性阶段)恶心和呕吐最有效的止吐药类别之一,通过阻断血清素与其受... 查看详情
20
2月
欧盟批准ENHERTU(德曲妥珠单抗)用于新辅助治疗后HER2阳性早期乳腺癌的维持治疗
2026年02月19日,欧洲药品管理局已批准ENHERTU(德曲妥珠单抗)的II类变更上市许可申请,该药物可作为单药疗法,用于治疗接受新辅助HER2靶向治疗后仍有残留浸润性疾病的HER2阳性乳腺癌成年患者,其中HER2阳性判定标准为免疫组化3+或原位杂交+。 ENHERTU是一种专门针对HER2的DXd抗体药物偶联物,其核心设计是通过四肽可裂解连接子,将HER2单克隆抗体与多个拓扑异构酶I抑制剂有效载荷连接而成,具备靶向性强、作用机制明确的特点,其药物抗体比均一且较高,约为每个抗体结合8个细胞毒性药物分子,这种结构可实现细胞毒性药物的靶向递送,同时保证其在血浆中的稳定性,且能被肿瘤细胞中高表达... 查看详情
20
2月
欧盟批准Anktiva联合卡介苗用于非肌层浸润性膀胱癌原位癌
2026年2月18日,ImmunityBio公司宣布,欧盟委员会已授予Anktiva联合卡介苗用于治疗成人卡介苗无反应性非肌层浸润性膀胱癌原位癌的有条件上市许可,无论患者是否伴有乳头状肿瘤。此次批准覆盖所有27个欧盟成员国以及冰岛、列支敦士登和挪威,使Anktiva在自美国食品药品监督管理局首次批准后不到两年内,已在四个监管辖区的33个国家获得批准,建立起全球商业布局。 Anktiva的通用名称为nogapendekin alfa inbakicept,其活性成分为nogapendekin alfa inbakicept,属于白细胞介素-15受体激动剂,作用机制为通过刺激CD4+T细胞、CD8... 查看详情
19
2月
美国FDA批准ACCRUFeR(麦芽酚铁)用于10岁及以上儿童缺铁性贫血
2026年02月17日,Shield Therapeutics宣布ACCRUFeR(ferric maltol,麦芽酚铁)获FDA批准,用于10岁及以上儿童缺铁性贫血的治疗。Accrufer是首个且唯一获批针对该儿童患者群体的口服处方铁剂。该药物于2019年首次获批用于成人铁缺乏症。 铁缺乏症是贫血最常见的病因,由于机体铁储备不足以支持血红蛋白合成所致。血红蛋白是红细胞内携带氧气的蛋白质。缺铁性贫血可表现为疲劳、面色苍白和头晕。病因包括胃肠道疾病引起的失血、月经、铁吸收障碍以及膳食摄入不足。 美国约有240万儿童受铁缺乏症影响。青少年人群风险升高,12至21岁女性中高达40%可能受累,主要由于... 查看详情
18
2月
美国批准WAKIX(替洛利生)用于发作性睡病引起的猝倒症治疗
2026年2月17日,美国食品和药物管理局批准了Harmony Biosciences公司的补充新药申请,将WAKIX(Pitolisant,替洛利生)片剂的适应症扩展至治疗6岁及以上发作性睡病患儿的猝倒症。此次批准后,WAKIX成为美国首个也是唯一一个获批用于治疗成人和儿童发作性睡病(无论是否伴有猝倒症)的非管制类治疗药物。 WAKIX是一种首创的选择性组胺H3受体拮抗剂/反向激动剂,其确切作用机制尚未完全明确,但其治疗效果被认为是通过阻断突触前H3受体,从而增加大脑中枢神经系统中促醒神经递质组胺的合成和释放来介导的。与许多其他发作性睡病治疗药物不同,WAKIX不属于管制类物质,这在儿科临床... 查看详情