29
1月
注意力缺陷多动障碍(多动症)药物Centanafadine获FDA优先审评
美国食品药品监督管理局(FDA)已受理centanafadine的新药申请(NDA),并将其纳入优先审评范围。Centanafadine是一款处于研究阶段的每日一次缓释胶囊,适用于儿童、青少年及成人注意力缺陷多动障碍(ADHD,又称为多动症)的治疗。FDA依据《处方药使用者付费法案》(PDUFA),为该药物设定的目标审评决定日期为2026年7月24日。 Centanafadine属于去甲肾上腺素、多巴胺及5-羟色胺再摄取抑制剂(NDSRI),这类药物在注意力缺陷多动障碍治疗领域属于首创类别,能够显著减轻注意力缺陷多动障碍(ADHD)的核心症状。此次提交的新药申请,主要依托四项关键的III期临床... 查看详情
29
1月
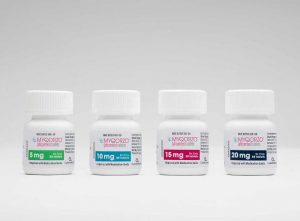
Myqorzo在美国上市用于梗阻性肥厚型心肌病治疗
2026年1月27日,梗阻性肥厚型心肌病治疗药物Myqorzo(通用名:aficamten)正式在美国上市,供处方使用。该药物此前于2025年12月获得美国食品药品监督管理局(FDA)批准,用于治疗成人症状性梗阻性肥厚型心肌病(oHCM),以改善患者的功能能力和临床症状。 Myqorzo为口服片剂,规格包括5毫克、10毫克、15毫克和20毫克,推荐每日服用一次,可与食物同服或空腹服用,需整片吞服。其起始剂量为每日5毫克,治疗开始后需根据患者左心室射血分数(LVEF)和瓦氏动作左心室流出道梯度(LVOT-G)评估结果,每2至8周考虑调整剂量,每次可增加5毫克,直至达到维持剂量或每日20毫克的最大... 查看详情
28
1月
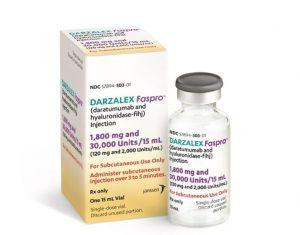
美国FDA批准皮下注射达雷木单抗DARZALEX FASPRO四联疗法用于不适合移植新诊断多发性骨髓瘤
2026年1月27日,美国食品药品监督管理局批准DARZALEX FASPRO(达雷木单抗和透明质酸酶-fihj)联合硼替佐米、来那度胺和地塞米松(四联疗法,简称D-VRD),用于治疗不适合自体干细胞移植的新诊断多发性骨髓瘤成年患者。 DARZALEX FASPRO的活性成分为达雷木单抗,这是一种靶向CD38的人源单克隆抗体,CD38蛋白在多发性骨髓瘤细胞表面大量表达。制剂中添加的透明质酸酶可实现皮下给药,相较于传统静脉注射方式,给药更为便捷。此次获批的四联疗法中,硼替佐米为蛋白酶体抑制剂,通过阻断蛋白酶体功能诱导肿瘤细胞凋亡;来那度胺为免疫调节剂,可调控免疫反应及肿瘤微环境相互作用;地塞米松... 查看详情
28
1月
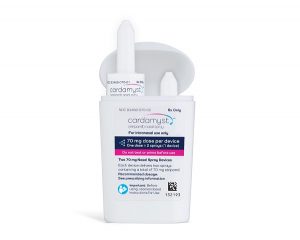
美国上市鼻喷雾剂Cardamyst用于阵发性室上性心动过速
Cardamyst(通用名:etripamil,依曲帕米)鼻喷雾剂已于2026年1月26日正式在美国零售药店上市,这是首款且唯一经美国FDA批准用于阵发性室上性心动过速(PSVT)成人患者的可自行给药鼻喷雾剂,也是30多年来FDA批准的首款PSVT治疗新药。 作为一种速效钙通道阻滞剂,Cardamyst的作用机制为抑制钙离子穿过房室结细胞、动脉平滑肌细胞及心肌收缩细胞的细胞膜内流,通过阻断房室结的折返,快速终止PSVT发作,使患者恢复窦性心律。其鼻喷雾剂型设计打破了传统静脉制剂需急诊注射的局限,允许患者在无医疗监护的情况下自行给药,适用于院外PSVT急性发作时的急救。 该药品为处方药,以纸盒包... 查看详情
28
1月
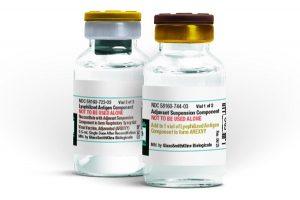
呼吸道合胞病毒(RSV)疫苗Arexvy获欧盟批准适用于18岁及以上成年人
欧盟委员会批准Arexvy用于18岁及以上成人,此举拓展了呼吸道合胞病毒疫苗市场,也标志着成人免疫策略的应用范围进一步扩大。 含佐剂重组呼吸道合胞病毒疫苗Arexvy已获得欧盟委员会批准,扩大适应症范围,覆盖欧盟及欧洲经济区所有18岁及以上成人。该疫苗此前已获批用于60岁及以上成人,以及50至59岁患重症风险较高的成人,此次适应症拓宽后,可面向全人群成人接种。 欧盟地区每年约有15.8万名18岁及以上成人因呼吸道合胞病毒相关疾病住院治疗,相较于儿童病例,成人出现重症并发症及接受高费用治疗的风险更高。此次获批为欧洲公共卫生系统及临床医生提供了更广泛的呼吸道合胞病毒预防选择,该疫苗同时也在推进全球... 查看详情
28
1月
糖尿病药物吸入胰岛素粉末Afrezza获FDA批准更新起始剂量指南
2026年1月26日,美国食品药品监督管理局批准更新吸入人胰岛素粉末(Afrezza)的标签,为1型糖尿病患者从每日多次注射或胰岛素泵餐时治疗转换时提供起始剂量指导。 此项决定部分得到了INHALE-3期试验结果的支持,该试验强调了使用此转换剂量改为吸入胰岛素后餐后血糖结果的改善。在试验期间,转换为吸入胰岛素的患者在第30周时糖化血红蛋白低于7%,较基线增加了100%。 更新的指南建议,如果当前皮下餐时胰岛素剂量小于等于3单位,则起始吸入胰岛素剂量为4单位;餐时胰岛素剂量为4-5单位对应起始吸入胰岛素剂量8单位;餐时胰岛素剂量为6-7单位对应吸入胰岛素12单位;餐时胰岛素剂量大于等于8单位则对... 查看详情
27
1月
阿尔茨海默病药物LEQEMBI IQLIK皮下注射起始剂量获FDA优先审评
2026年1月25日,美国食品药品监督管理局(FDA)已接受针对LEQEMBI® IQLIKTM(lecanemab-irmb)皮下注射作为早期阿尔茨海默病起始剂量的补充生物制剂许可申请,并授予其优先审评资格。 2026年1月25日,东京与马萨诸塞州剑桥消息——卫材有限公司与百健公司今日共同宣布,FDA已接受卫材提交的关于lecanemab-irmb(美国商品名:LEQEMBI)皮下自动注射器(SC-AI)LEQEMBI IQLIK作为每周一次起始剂量的补充生物制剂许可申请(sBLA)。LEQEMBI适用于治疗处于轻度认知障碍或轻度痴呆阶段的阿尔茨海默病(统称为早期阿尔茨海默病)。该申请已被授... 查看详情
26
1月
FDA授予Gotistobart治疗鳞状非小细胞肺癌孤儿药指定
Gotistobart获美国食品药品监督管理局(FDA)孤儿药认定,适用人群为鳞状非小细胞肺癌(NSCLC)患者。该药物是一种新型肿瘤微环境选择性、靶向细胞毒性T淋巴细胞相关抗原4(CTLA-4)的调节性T细胞耗竭候选药物,专门用于治疗鳞状非小细胞肺癌。目前,该药物正处于关键的Ⅲ期PRESERVE-003试验(试验编号NCT05671510)阶段,研究对象为转移性鳞状非小细胞肺癌患者。 尽管程序性死亡受体(PD)-(配体)1抑制剂已改善无癌基因驱动疾病的转移性非小细胞肺癌患者的预后,但仍有相当一部分患者使用后仅能实现暂时性疾病控制,甚至无法控制病情。此外,CTLA-4虽已被证实是免疫检查点抑制... 查看详情
23
1月
GAMMAGARD LIQUID ERC在美国上市用于原发性免疫缺陷治疗
2025年1月22日,武田公司在美国推出GAMMAGARD LIQUID ERC,这是目前唯一一款低免疫球蛋白A含量且即用型液态免疫球蛋白疗法。该产品中免疫球蛋白A含量低于或等于2微克/毫升(10%溶液),已获批准作为替代疗法,用于两岁及以上原发性免疫缺陷患者。 GAMMAGARD LIQUID ERC是一款无需复溶的即用型液态免疫球蛋白疗法,其免疫球蛋白A含量低于或等于2微克/毫升(10%溶液),可通过静脉或皮下途径给药。该产品采用了与武田其他液态免疫球蛋白产品相同的生产工艺,并具备增强型去除能力以降低免疫球蛋白A含量。现有两种规格的液体西林瓶包装:5克/50毫升和10克/100毫升。产品可... 查看详情
23
1月
Targretin(贝沙罗汀):治疗皮肤T细胞淋巴瘤的靶向药物
贝沙罗汀Bexarotene(商品名:Targretin)属于类视黄醇药物,1999年以孤儿药身份获得美国FDA批准,目前已在全球36个国家和地区投入临床,核心用于治疗皮肤T细胞淋巴瘤这一罕见病症。凭借独特作用机制与明确疗效,它被美国国立综合癌症网络、欧洲癌症研究与治疗组织等国际权威指南纳入推荐方案,成为复发性皮肤T细胞淋巴瘤的标准治疗药物之一。2024年7月,贝沙罗汀正式登陆中国香港和澳门地区,为当地患者带来新的治疗选择,其在中国大陆的临床试验也已获批,正稳步推进中。 Targretin的作用机制与适应症 Targretin(贝沙罗汀)属于一类被称为选择性维甲酸X受体激动剂的药物。它与人体细... 查看详情