01
4月
欧盟批准Kygevvi(脱氧胞苷/脱氧胸苷)用于胸苷激酶2缺乏症治疗
2026年3月31日,欧盟委员会正式批准优时比(UCB)公司的Kygevvi(doxecitine/doxribtimine,通用名:脱氧胞苷/脱氧胸苷)上市,用于治疗症状发作年龄在12岁及以下、经基因确诊的胸苷激酶2缺乏症(TK2d)儿童与成人患者。该药物是全球首款且唯一获批用于TK2d的针对性治疗药物。 Kygevvi为2g/2g规格的口服溶液用粉末,活性成分为脱氧胞苷与脱氧胸苷European Medicines Agency。其作用机制为将两种核苷成分掺入骨骼肌线粒体DNA,恢复线粒体DNA拷贝数,进而改善TK2d患者的骨骼肌功能European Medicines Agency。 本... 查看详情
01
4月
FDA受理Lirafugratinib用于FGFR2融合/重排胆管癌的新药申请并授予优先审查资格
2026年3月30日,美国食品药品监督管理局(FDA)受理Elevar Therapeutics公司提交的Lirafugratinib新药申请(NDA),并授予其优先审查资格,用于治疗既往接受过治疗、携带FGFR2融合或重排的胆管癌(CCA)患者,FDA设定的处方药用户付费法案(PDUFA)目标审评日期为2026年9月27日。 Lirafugratinib(研发代号:RLY-4008)是一种高效、选择性口服小分子不可逆FGFR2抑制剂,通过与FGFR2激酶结构域半胱氨酸491(Cys491)形成不可逆共价键,特异性抑制FGFR2信号通路,其对FGFR2的选择性显著高于FGFR家族其他成员。临床... 查看详情
31
3月
美国FDA批准Prolia(地舒单抗)生物类似药Ponlimsi ,并受理Xolair生物类似药上市申请
2026年3月30日,美国FDA批准梯瓦制药(Teva)的Ponlimsi(denosumab-adet)作为安进(Amgen)Prolia(地舒单抗)的生物类似药上市,同时接受梯瓦制药提交的Xolair(奥马珠单抗)生物类似药的生物制品许可申请(BLA)审查Teva Pharmaceuticals。 Ponlimsi为RANK配体(RANKL)抑制剂类生物类似药,其获批基于全面的分析与临床证据,数据显示该药物在疗效、安全性及免疫原性方面与原研药Prolia高度相似,无临床意义上的差异。此次获批覆盖Prolia在美国已获批的全部适应症,包括治疗骨折高风险的绝经后骨质疏松症女性、骨折高风险的男性... 查看详情
31
3月
美国FDA取消1毫克肾上腺素鼻喷雾剂Neffy用于I型过敏反应治疗的年龄限制
2026年3月27日,美国食品药品监督管理局(FDA)正式批准更新Neffy(epinephrine nasal spray,肾上腺素鼻喷雾剂)1毫克剂量的处方信息,核心调整为取消该剂量此前设定的年龄限制,进一步扩大了该剂量的适用人群范围,为I型过敏反应的紧急治疗提供了更灵活的用药选择。 Neffy作为一款肾上腺素鼻喷雾剂,其核心成分是肾上腺素,这是一种用于紧急缓解I型过敏反应(包括危及生命的过敏性休克)的关键药物,能够快速作用于身体,缓解气道水肿、呼吸困难、血压下降等严重过敏症状,为患者争取后续治疗时间。此次标签更新前,Neffy 1毫克剂量仅被批准用于体重33磅至66磅(约15公斤至30公... 查看详情
31
3月
欧盟批准Tryngolza(Olezarsen)用于重度高甘油三酯血症治疗
2026年3月30日,欧洲药品管理局(EMA)正式受理并验证了Tryngolza(Olezarsen)用于治疗成人重度高甘油三酯血症(sHTG,甘油三酯水平≥880mg/dL,即≥10mmol/L)的适应症扩展申请。该药物此前已于2025年9月19日在欧盟获批,作为饮食辅助治疗用于经基因确诊的家族性乳糜微粒血症综合征(FCS)成人患者Ionis Pharmaceuticals, Inc.。 Tryngolza(Olezarsen)是一种靶向RNA的药物,其作用机制为抑制肝脏产生载脂蛋白C-III(apoC-III),而apoC-III是甘油三酯代谢的关键调控蛋白,通过降低其生成可显著减少体内甘... 查看详情
30
3月
DARZALEX(daratumumab,达雷妥尤单抗)在欧洲获批患者/照护者自行给药用于多发性骨髓瘤治疗
欧洲药品管理局人用药品委员会批准了达雷妥尤单抗皮下注射剂(DARZALEX,daratumumab)的一项II型标签变更,允许多发性骨髓瘤患者在经过专业医护人员评估适宜且接受规范培训后,从第五剂起自行或由照护者实施给药。 达雷妥尤单抗由此成为欧洲首个获批可自行注射的肿瘤治疗药物。此次标签更新覆盖了该药此前在欧洲获批的全部适应症。在欧洲,达雷妥尤单抗获批用于以下治疗场景: 联合来那度胺和地塞米松,或联合硼替佐米和地塞米松,用于治疗既往接受过至少一线治疗的多发性骨髓瘤成人患者; 联合泊马度胺和地塞米松,用于治疗既往接受过包含蛋白酶体抑制剂和来那度胺的一线治疗后出现来那度胺耐药的多发性骨髓瘤成人患者... 查看详情
30
3月
美国FDA加速批准基因疗法Kresladi用于重度白细胞粘附缺陷症I型治疗
2026年3月27日,美国食品药品监督管理局(FDA)加速批准Rocket Pharmaceuticals公司开发的自体造血干细胞基因疗法Kresladi(marnetegragene autotemcel)上市,用于治疗因ITGB2基因双等位基因变异导致的严重白细胞粘附缺陷症I型(LAD-I)儿科患者,且患者无人类白细胞抗原(HLA)匹配的同胞供体可进行异基因造血干细胞移植。这是FDA批准的首款针对严重LAD-I的基因疗法。 Kresladi是一种一次性自体造血干细胞基因疗法,其作用机制为从患者自身采集CD34+造血干细胞,通过慢病毒载体导入功能正常的ITGB2基因进行体外修饰,经预处理后以... 查看详情
30
3月
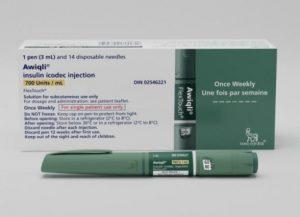
FDA批准诺和诺德长效基础胰岛素Awiqli每周一次用于成人2型糖尿病
2026年3月27日,丹麦诺和诺德公司宣布,美国食品药品监督管理局(FDA)已批准Awiqli®(insulin icodec-abae,依柯胰岛素注射液,700单位/毫升)上市。该药物是全球首款且唯一一款每周一次给药的长效基础胰岛素,适应症为作为饮食和运动的辅助手段,改善成人2型糖尿病患者的血糖控制。 Awiqli®的获批基于ONWARDS 3a期临床试验项目的结果。该项目包含四项随机、活性对照、目标治疗试验,共纳入约2680名血糖控制不佳的成人2型糖尿病患者。研究中,Awiqli®可与餐时胰岛素联用,或与常用口服降糖药和/或GLP
1受体激动剂联合使用。临床数据显示,Awiqli®在降低糖... 查看详情
27
3月
瑞士批准PEDMARK(硫代硫酸钠)用于预防儿童及青少年铂化疗造成的听力损失
2026年3月26日,瑞士药品监督管理局(Swissmedic)正式批准PEDMARK(通用名:硫代硫酸钠,商品名在欧洲为Pedmarqsi)上市,用于预防1月龄至18岁、患有局限性非转移性实体瘤的患者,在接受顺铂化疗时引发的听力损失(耳毒性)。这是瑞士境内首个且唯一获批用于该适应症的药物,填补了儿童顺铂化疗耳毒性预防领域的治疗空白。 PEDMARK的活性成分为硫代硫酸钠,是一种静脉输注制剂,其获批基于两项国际多中心、开放标签、随机对照的Ⅲ期临床试验——SIOPEL 6与COGACCL0431的关键数据。SIOPEL 6试验纳入114例标准风险肝母细胞瘤患儿,随机接受顺铂联合PEDMARK或单... 查看详情
26
3月
美国FDA加速批准酶替代疗法Avlayah用于亨特综合征治疗
2026年3月25日,美国食品药品监督管理局(FDA)加速批准Avlayah(通用名:tividenofusp alfa-eknm)用于治疗亨特综合征(黏多糖贮积症II型,MPS II),适用于体重至少5公斤、在出现严重神经功能损害前处于症状前或有症状阶段的儿科患者,用于治疗其神经病变表现。 Avlayah是一款酶替代疗法,由艾杜糖-2-硫酸酯酶(IDS)与DenaliTherapeutics的酶转运载体(ETV)融合而成,通过与血脑屏障上的转铁蛋白受体结合,借助受体介导的转胞吞作用穿越血脑屏障,将IDS递送至中枢神经系统,以缓解亨特综合征的中枢神经系统症状。 本次加速批准基于脑脊液硫酸乙酰肝... 查看详情